有色溶解有机物吸光
从水生生态学的角度来看,土壤腐殖质物质的意义在于,当水以降雨的形式通过土壤排入河流和湖泊,最终进入河口和海洋时,它从土壤中提取出一些水溶性腐殖质物质,这些物质使水呈现黄色,对生态环境产生重大影响光吸收尤其是在光谱的蓝色一端。美国的James和Birge(1938)和奥地利的Sauberer(1945)进行了广泛的定量研究吸收光谱有不同程度的黄色湖水。腐殖质的颜色是由于存在多个双键,其中许多是共轭的,一些在芳核中。在腐殖质材料的任何样品中,都有许多不同的发色团,因此有许多电子激发水平,由于它们重叠,产生了相当无差别的紫外/可见吸收光谱。Visser(1984)在魁北克针叶林集水区的地表水中发现
(加拿大),每单位质量的腐殖酸的颜色强度几乎是黄腐酸的四倍:然而,它的浓度只有黄腐酸的七分之一,这意味着在这些水域中,腐殖酸贡献了大约三分之一的颜色,而黄腐酸贡献了三分之二的颜色。在自然水体中溶解的腐殖质材料在吸收光的同时,在蓝色区域具有较宽的荧光发射带。
的光吸收这些溶解的腐殖质物质在天然内陆水域的性质可以比较容易地通过测量来确定吸收光谱在5厘米或10厘米通路长度的细胞中过滤(0.2-0.4毫米孔径)的水样图3.5显示了该物质在澳大利亚一些内陆水域的吸收光谱。这些是典型的腐殖质吸收光谱,在可见光谱的红端吸收非常低或不存在,并随着波长向蓝色方向的减小而稳步上升:在紫外线区域的吸收仍然更高。
在内陆水域中溶解的黄色物质的存在往往很容易被眼睛看到。它在海水中的存在(其浓度要低得多)并不那么明显,卡勒(1937,1966)也指出了它在这些生态系统中的重要作用。图3.5还显示了可溶性黄色物质在河口和沿海水域的吸收光谱。
天然水中溶解的黄色物质被称为“黄色物质”、“gelbstoff”(德语中同名)、“黄色有机酸”、“腐木酸”、“黄腐酸”、“腐殖酸”等。不同水体中溶解的黄色物质不仅分子大小不同,化学成分也不同。671,1314,1315在光衰减的背景下,有一个通用的名称将是有用的,适用于所有或任何这些化合物,而不管它们的化学性质如何,它只是表明它们优先吸收光谱蓝色端的光。“黄色物质”或“gelbstoff”太非特异性,可能适用于从黄油到氯化铁的任何东西。我建议用“gilvin”这个词,它是一个名词,源于拉丁形容词gilvus,意思是淡黄色。696'Gilvin' would thus be defined as a general term to be applied to those soluble yellow substances, whatever their chemical structure, which occur in natural waters, fresh or marine, at concentrations sufficient to contribute significantly to the attenuation of PAR. While 'gilvin' is certainly to be found in the aquatic literature, it is nevertheless true that the term that is most commonly used in recent papers is the acronym CDOM (pronounced 'seedom'), which is taken to stand for either coloured dissolved organic matter, or chromophoric dissolved organic matter. In recognition of
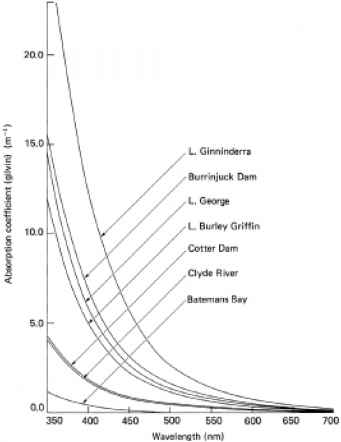
图3.5可溶性黄色物质(gilvin, CDOM)在澳大利亚各天然水域的吸收光谱(来自Kirk, 1976b)。最低的曲线(新南威尔士州的贝特曼斯湾)是河口附近的沿海海水;下一个弯道(克莱德河,新南威尔士州)是一个河口;剩下的是内陆水体在新南威尔士州/澳大利亚首都地区的南部高地。纵坐标尺度对应于真实的原位吸收系数,由于吉尔文。
图3.5可溶性黄色物质(gilvin, CDOM)在澳大利亚各天然水域的吸收光谱(来自Kirk, 1976b)。最低的曲线(新南威尔士州的贝特曼斯湾)是河口附近的沿海海水;下一个弯道(克莱德河,新南威尔士州)是一个河口;其余是新南威尔士州/澳大利亚首都地区南部高地的内陆水体。纵坐标尺度对应于真实的原位吸收系数,由于吉尔文。
这是一种常见的用法,但不影响其隐含的解释,在本书的其余部分,我将交替使用“CDOM”和“gilvin”来表示天然水中溶解的黄色物质。
从图3.5的吸收光谱可以看出,CDOM的浓度不仅在海洋和淡水之间存在显著差异,在不同的内陆水域之间也存在显著差异。可以用来表示CDOM浓度的一个方便的参数是这种物质在水中440nm处的吸收系数:我们将用g440表示。之所以选择这个波长,是因为它大约对应于大多数藻类在光合作用中所具有的蓝色波段峰值的中点光谱.
在许多水域,当然是内陆水域,CDOM吸收足够高,使用50或100毫米径长的电池可以以合理的精度测量g440。当CDOM吸收较低时,如在大多数海水中,可以用等效路径长度非常长的ICAM或PSICAM类型(§3.2)的吸收计或反射管吸收计在滤液上测量吸收系数。另外,可以在吸收较高的近紫外(350-400 nm)中进行测量,g440由典型CDOM吸收光谱的比例确定,或使用近似关系
a(l) = a(20)e~S(1~l0) (3.5)
其中a(l)和a(10)分别是波长l和10 nm处的吸收系数,S是描述吸收曲线.Babin等人(2003b)在欧洲各地沿海水域(英吉利海峡、亚得里亚海、波罗的海、地中海和北海)的约350个监测站发现,S在0.0176±0.0020 nm-1左右的狭窄范围内变化。新西兰的12个湖泊S在0.015 ~ 0.020 nm-1之间变化,平均为0.0187 nm-1;澳大利亚的285个内陆水域S在0.012 ~ 0.018 nm-1之间变化,平均为0.016 nm-1.720当CDOM发生部分光漂白时,残留的溶解色的光谱S值略高。1417与这一观察结果一致,Twardowski和Donaghay(2002)发现,在沿海峡湾,地表水的S值高于底水:他们提出,相对于沿海CDOM,通常与海洋CDOM相关的更高光谱斜率可能是由于累积光漂白的增加。
当被近紫外光(通常为~355nm或~370nm)激发时,CDOM会在蓝色区域发出一个非常宽的荧光峰。量子率约为0.8%这种荧光在天然水中的强度被发现与CDOM的吸收高度相关,它可以用作测量CDOM的另一种方法,可以在水中使用潜水荧光计,也可以通过机载激光远程激发荧光(见第7章)。1418,94
表3.2以g440值的形式列出了各地理区域的海洋和淡水的精选公布数据。
表3.2由于溶解色(g44o)和颗粒(浮游植物+非生物性浮游物)颜色(p440)。在进行了多次测量的情况下,在某些情况下指出了平均值、标准偏差、范围和所涵盖的时间周期。对于某些水,只有CDOM加颗粒(g + p)的吸收系数可用。
一、大洋水域
大西洋
马尾藻海
从百慕大
加勒比海
墨西哥湾-墨西哥湾环侵入罗马奇毛里塔尼亚深部上升流几内亚湾太平洋加拉波戈斯群岛加拉波戈斯群岛太平洋中部秘鲁外海印度洋寡营养水中营养水富营养化水地中海北冰洋西部波弗特海和楚科奇海南部大洋南北样带,42-55°S,沿142°E
2大陆架、海岸和河口水域
墨西哥湾尤卡坦陆架坎佩切湾的圣布拉斯角密西西比羽北美洲,大西洋沿岸
新英格兰大陆架,夏季,美国东南部,乔治亚州,离岸60公里,1993年春(河水流量高)1992年夏罗德岛河口
0.024 - -0.113
0.01
0.13
760 616 636 204
636 161 161
189 636 636 189
748 748 748
1439
204 204 204 204 204
1269 980
980 428
表3.2(续) |
|||
水体 |
g44o (m 1) |
P440 (m *) |
参考 |
切萨皮克湾(罗得州 |
0.27 |
0.80 |
428 |
r .嘴) |
|||
佐治亚盐沼 |
1.52 |
- |
1460 |
阿拉伯海 |
|||
印度科钦,3公里 |
0.24c (g + p) |
雷竞技csgo1113 |
|
离岸 |
|||
离岸30公里 |
0.10c(g + p) |
雷竞技csgo1113 |
|
孟加拉湾 |
|||
恒河口附近 |
0.37 |
- |
745 |
黄海 |
0.20 - -0.23一个 |
- |
574 |
东太平洋 |
|||
0.29 |
745 |
||
南太平洋 |
|||
查塔姆高地(纽 |
0.044 |
0.026 |
1218 |
西兰),共有19个站 |
|||
北大西洋/北海/波罗的海 |
|||
系统 |
|||
w .格陵兰岛 |
0.004 |
- |
574 |
北大西洋 |
0.02 |
- |
670 |
冰岛 |
0.016 |
- |
574 |
Orkney-Shetland |
0.016 |
- |
574 |
北海(Fladen Ground) |
0.03 - -0.06一个 |
- |
574 |
瓦登海 |
-3.0 ~ 0.64 (0.0) |
- |
583 |
斯卡格拉克海峡 |
0.05 - -0.12一个 |
- |
574 |
卡特加特海峡 |
0.12 - -0.27一个 |
- |
574 |
丹麦,奥胡斯湾 |
0.232 |
834 |
|
(卡特加特海峡) |
|||
波罗的海 |
0.36 - -0.42一个 |
- |
574 |
南波罗的海 |
0.26 |
- |
636 |
Bothnian海湾 |
0.41 |
- |
636 |
苏格兰的爱提湖 |
0.7 - -1.0 |
- |
887 |
地中海 |
|||
Villefranche湾 |
0.060 - -0.161一个 |
- |
161 |
马赛排水口 |
0.074 - -0.646一个 |
- |
161 |
R.瓦尔口 |
0.136 |
- |
161 |
罗纳口 |
0.086 - -0.572一个 |
- |
161 |
伊特鲁里亚海 |
|||
那不勒斯湾 |
0.02 - -0.20一个 |
- |
391 |
北亚得里亚海 |
|||
Sacca di Goro (R. Po口) |
0.32 - -3.43一个 |
- |
391 |
威尼斯泻湖 |
0.44 - -0.73一个 |
- |
391 |
黑海 |
|||
克里米亚半岛(沿海) |
0.081-0.197b (av. 0.13) |
- |
311 |
澳大利亚东南部 |
|||
(a)杰维斯湾 |
|||
3站 |
0.09 - -0.14一个 |
0.03 - -0.04 |
720 |
水体 |
G440 (m 1) |
P440 (m 1) |
参考 |
(b)塔斯曼海/克莱德R.系统 |
|||
塔斯曼海 |
0.02 |
- |
697 |
贝特曼湾 |
0.18 |
- |
696 |
克莱德河口 |
0.64 |
- |
697 |
(c)吉普斯兰(河口)湖 |
|||
系统 |
|||
l .王 |
0.58 |
0.25 |
720 |
l .维多利亚 |
0.65 |
0.22 |
720 |
l .惠灵顿 |
1.14 |
2.27 |
720 |
拉筹伯R。 |
1.89 |
2.78 |
720 |
塔斯马尼亚(d) |
|||
Huon R.河口口 |
0.16 - -0.30 |
- |
241 |
东北澳大利亚/大 |
|||
大堡礁 |
|||
大堡礁,南纬-18° |
0.050±0.028 |
0.010 |
126 |
Mossman-Daintree河口, |
0.082±0.087 |
0.085 |
126 |
16°s,旱季 |
|||
湿季 |
0.246±0.254 |
0.531 |
126 |
Fitzroy R./吉宝湾系统, |
0.471 |
- |
1025 |
23°S。干燥的季节。河口 |
|||
站2 |
|||
离岸28公里 |
0.006 |
- |
1025 |
澳大利亚西部 |
|||
Swan R.河口: |
|||
距河口上游7公里 |
0.66 (0.09 - -2.95) |
749 |
|
上游39公里 |
3.82 (2.21 - -10.6) |
749 |
|
新西兰 |
|||
南岛,11个陆架站 |
0.04-0.10 (av. 0.07) |
- |
283 |
北岛,9个河口, |
0.1 - -0.6 |
- |
1401 |
河口处,低潮 |
|||
日本,太平洋沿岸 |
|||
下田17公里 |
0.024 |
0.133 |
727 |
下田5公里 |
0.011 |
0.095 |
727 |
Nabeta湾 |
0.054 |
0.140 |
727 |
北海道芳卡湾 |
0.065 |
- |
1171 |
3内陆水域 |
|||
欧洲 |
|||
莱茵R。 |
0.48 - -0.73一个 |
- |
574 |
Donau R.,奥地利 |
0.85 - -2.02 |
- |
574 |
Ybbs R.,奥地利 |
0.16 |
- |
574 |
Neusiedlersee、奥地利 |
~2.0±0.4 |
- |
314 |
(8个月) |
1.4 - -2.8 |
- |
|
Blaxter L.(沼泽湖),英国 |
9.65 |
- |
891 |
爱尔兰: |
|||
Carmean采石场 |
0.23 |
- |
643 |
Killea水库 |
0.5 |
- |
643 |
表3.2(续) |
||||
水体 |
g44o (m 1) |
P440 (m 1) |
参考 |
|
内伊湖 |
1.9 |
- |
643 |
|
湖有限元分析 |
4.7 |
- |
643 |
|
湖白尾海雕 |
5.3 |
- |
643 |
|
Loughnagay |
6.4 |
- |
643 |
|
湖Bradan |
17.4 |
- |
643 |
|
湖Napeast |
19.1 |
- |
643 |
|
苏格兰的利文湖 |
1.2 |
- |
1336 |
|
山地湖泊(阿尔卑斯山, |
||||
庇里牛斯山): |
||||
主要是岩石 |
0.074 av。 |
- |
776 |
|
集雨 |
(0.00 - -0.28) |
|||
高山草甸 |
0.154 av。 |
- |
776 |
|
集雨 |
(0.09 - -0.21) |
|||
森林集水区 |
0.232 av. (0.02-0.53) |
- |
776 |
|
非洲 |
||||
L.乔治,乌干达 |
3.7 |
- |
1336 |
|
L.维多利亚(乌干达), |
0.45 |
1013 |
||
默奇森湾 |
||||
北美 |
||||
水晶L.,威斯康辛州。美国 |
0.16 |
- |
620 |
|
威斯康辛州阿德莱德市。美国 |
1.85 |
- |
620 |
|
Otisco L.,纽约,美国 |
0.27 |
0.27 |
1446 |
|
安大略铁石湾, |
0.90 |
0.65 |
1445 |
|
美国 |
||||
伊利湖 |
0.23 (0.08 - -0.75) |
- |
116 |
|
虚张声势的L., n.s.,加拿大 |
0.94 |
- |
495 |
|
宾治碗,美国,加拿大 |
6.22 |
- |
495 |
|
南美 |
||||
委内瑞拉的古里水库 |
4.84 |
- |
805 |
|
Carrao R.,委内瑞拉 |
12.44 |
- |
805 |
|
中国 |
||||
l .天目 |
0.48±0.24 |
- |
1501 |
|
日本 |
||||
l . Kizaki |
0.30 |
0.71 |
727 |
|
l . Fukami-ike |
0.85 |
3.11 |
727 |
|
澳大利亚 |
||||
(a)南部高地 |
||||
销大坝 |
1.28 - -1.46 |
0.77 |
701年,720年 |
|
Corin大坝 |
1.19 - -1.61 |
0.11 |
701年,720年 |
|
l . Ginninderra |
1.54±0.78 |
0.16 - |
0.58 |
696, 697, 701, 720 |
(3年) |
0.67 - -2.81 |
- |
||
l·乔治。 |
1.80±1.06 |
3.73 - |
4.21 |
696, 697, 701, 720 |
(5年) |
0.69 - -3.04 |
Burrinjuck Dam 2.21±1.13 0.63-1.44 古公坝3.42 0.83 奎恩贝安R. 2.42 - Molonglo R. 0.44 - 在汇流1.84以下 quanbeyan R。 从沼泽到集水区的小溪 (b)墨累-达令体系 Murrumbidgee R., Gogeldrie 0.4-3.2 - 堰(10个月) L.维安根1.13 0.38 格里菲斯水库1.34 3.73 贫瘠的盒子沼泽1.59 2.55 主管,MIA 1.11 5.35 主排水管,MIA 2.12 10.34 Murray R.,上游0.81-0.85 - 亲爱的融合 达令R,与默里汇合点0.7-2.5以上 (c)北领地(马杰拉溪溪涧) 木金芩1.11 1.13 古朗古尔2.28 1.68 乔治城1.99 18.00 塔斯马尼亚(d) Huon R. 7-14 -湖泊: 佩里0.06 - 女士塔恩0.40 - 里斯登布鲁克0.98 - 巴林顿3.05 - -戈登8.29 (e)昆士兰东南部沿海沙丘湖 L.布曼津2.59 - L.库鲁美拉14.22 - (f)南澳大利亚 Bold山5.40 2.25水库 696 697 701 720 701 720 720 720 1014 720 720 720 720 720 720 1014 1014 725 725 725 152 152 152 152 152 152 152 151 151 151 151 新西兰 怀卡托R.(330公里,L. Taupo到海):L. Taupo(0公里)Ohakuri(77公里)Karapiro(178公里)Hamilton(213公里)Tuakau(295公里)湖泊(11个月的月平均值):Rotokakahi Rotorua Opouri Hakanoa D . 0.070 0.22 0.82 0.97 1.37 0.033 0.32 0.71 0.98 1.67 282 282 282 282 282 285 285 285 285 285 a在波长小于440nm处测量的值,并根据适当的CDOM吸收光谱转换为g440。b在443 nm处进行测量,以符合相应的cseaifs波段。 c c在440 nm处经散射校正后的公布值。 这一汇编提供了自然水域中可能出现的典型吉尔文浓度的一些概念,但在世界上其他具有良好湖沼特征的地区,显然缺乏测量结果。从表3.2的数据可以看出,海水的溶解色一般要比内陆水少得多,而且离陆地越远,浓度越低。波罗的海的高浓度(海水)是值得注意的:随着海水中河水的比例减少,它从波斯尼亚湾向南下降。从克莱德河-贝特曼斯湾和拉特罗布河-吉普斯兰湖(澳大利亚)的数据中可以看出,河口系统中浓度随着距离上游海洋的距离而增加。大量流出彩色水的亚马逊河向热带北大西洋西部贡献了大量的CDOM,它对光学性质的影响在距离河口1000公里以上的地方都可以探测到 尽管gilvin的化学性质相当稳定——冷藏样品中的浓度在几周内通常只会有微小变化——但它在任何内陆水体中的浓度都随着时间的变化而发生变化,这与流域不同地区的降雨事件以及流入水中gilvin浓度的变化有关。表3.2中的一些数据表明了这种变化的程度。例如,在澳大利亚堪培拉的伯利格里芬湖(Lake Burley Griffin), g440的价值在五年期间变化了7倍。然而,对于任何给定的水体,变化确实倾向于在某个平均值附近,水体可以被视为典型的高、低或中等浓度。一个特定的湖泊,蓄水还是由河流瀑布决定的水系、植被、土壤和气候。raybet雷竞技最新 支配地表水中吉尔文浓度的因素还没有很好地了解,鉴于这种物质对水生初级生产的巨大影响,有必要了解更多。可以得出的一个概括是,来自沼泽或沼泽的排水水中的吉尔文浓度很高:例如,在北欧的泥炭沼泽中很容易看出这一点,并且在英国沼泽湖和澳大利亚南部高原沼泽地排水的小溪的g440值中得到了定量显示(表3.2)。吉尔文浓度也很高,从潮湿的热带如表3.2中委内瑞拉两个水域的g440值所示。在这些地区长期或经常浸水的土壤中,氧气的缺乏导致部分分解的有机物的积聚,而gilvin就是由这种有机物的可溶性成分衍生而来的。硬币的另一方面是,吉尔文地区富含石灰石的集水区的排水量往往较低。在北美,已经观察到湖水颜色与湖泊深度之间呈反比关系。植被类型、土壤矿物学、农业做法、气候和其他环境参数对吉尔文浓度的影响还没有很好地了解。raybet雷竞技最新 虽然,正如我们所注意到的,吉尔文在化学上是相当稳定的,但它确实在表层受到强烈阳光的光化学降解。已发现分解产物包括一系列低分子量羰基化合物,如丙酮酸、甲醛和乙醛,以及低分子量羧酸(草酸、丙二酸、甲酸和乙酸),所有这些都可被水生微生物利用。Kieber et al.(1990)根据其速率测量,估计海洋混合层中来自河流的溶解腐殖质的半衰期为5至15年。Mopper等人(1991)提供的证据表明,光化学途径实际上是海洋中长期存在的生物难降解溶解有机碳的主要降解途径。然而,微生物对CDOM的分解也很重要:在密西西比河羽流的水中,CDOM的分解速率约为光氧化速率的30% 虽然行动光谱表示UVB区域是太阳光谱(280-320纳米)对CDOM的损害最大,685这并不能得出结论,在自然水体中,通过水柱进行大部分光氧化的是UVB。CDOM对UVB的高吸收率确保了该光谱波段随着深度的增加而迅速衰减,因此在水柱深处发生的光氧化一定是由于波长较长的光。对于芬兰的一个腐殖质湖,Vahatalo等人(2000)计算出UVB对光化学矿化的贡献为9%,UVA (320-400 nm)为68%,可见光为23%。为阿根廷的湖泊和Pennsylvania, USA, Osburn et al.(2001)计算出UVB辐射与UVA和蓝光相比,CDOM对光漂白的影响较小(<20%)。南大西洋湾的大陆架水域(美国东南部), Miller等人(2002)的计算表明,太阳光谱的UVA区域是溶解有机质光氧化的主要原因。对于Chesapeake Bay (USA)的河口水域,Osburn et al.(2009)发现CDOM的长波光漂白随盐度的增加而增加。 在淡水水库的情况下,水的颜色可以是在使用前暴露在阳光下多长时间的函数。在澳大利亚北部的热带地区,Townsend等人(1996)发现,在两个集水区相似的相邻水库中,8年期间gilvin的平均浓度与滞留时间成反比。曼顿河水库的颜色通常是达尔文河水库的两到三倍,他们认为这是由于前水体的停留时间更短,因此光漂白的时间也更短。 由于水体中的总有机物质可能含有一些比例不定的无色有机物质,因此很难知道测量CDOM的比吸收系数(单位重量的吸收)有什么意义。对于丹麦沿海水域,Stedmon等人(2000)发现Skagerrak的0.0727 m2g_1C到Kattegat的0.630 m2g_1C,数据集平均值为0.29±0.11m2g_1 1c,在375 nm处。山为大量阿尔卑斯山的湖泊Pyrenees、Laurion等(2000)在0.43 ~ 3.51m2g~1C范围内,发现320 nm处总溶解有机碳的比吸收系数。表层水体的比吸收系数一般低于深层,这可能是由于光漂白造成的。 |
||
继续阅读:非生物性浮游物
这篇文章有用吗?