在溶液中反应
1。气态污染物与大气的相互作用水解决方案
由于气体性质的许多重要的主要和次要的污染物,大气反应动力学研究的重点在历史上一直在气相系统。然而,现在很清楚,反应发生在液相和固体和液体的表面上扮演了一个重要的角色在平流层臭氧损耗等问题(12和13章),酸雨,雾(7和8章)和气溶胶粒子的增长和属性(第9章)。因此,我们简要讨论在溶液中反应动力学在这一节和“异构”动力学部分E。
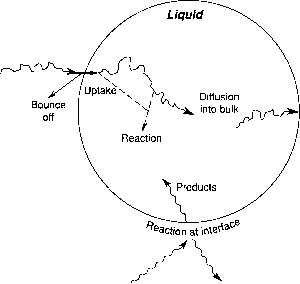
水相,作为反应介质在大气中存在的形式的云、雾、雨、和颗粒物组成的水溶液中含有污染物或电影周围的水不溶性核心(见第9章)。例如,在典型的相对湿度,~ 30 - 50%的气溶胶质量是由于水(Graedel和韦斯切勒,1981)。然而,许多物种的反应,被认为在这样大气的解决方案,例如,S02, 03年,H202,和氮氧化物排放或形成的气相。反应在溶液中发生之前,然后,几个步骤见图5.12必须首先发生:
(1)气体的扩散到表面的液滴
(2)运输的天然气在空气与接口
(3)溶剂化物种扩散的体相液滴
(4)反应的物种在水相或接口本身(见部分E.l)。
气体扩散快相对于水相扩散;即。相对于第三步,第一步是快。因此对气体扩散系数f atm压力0.1 ~ 1厘米2 s”1,而在液体~ 10”5厘米2 s”1对小分子。详细讨论了施瓦茨和弗赖堡(1981),气相扩散,在大多数(但不是所有)的情况下,将不会(即最慢。,速度决定)的步骤。
气体溶解在溶液中不同程度地取决于气体的性质。在足够长的时间,可以建立一个平衡之间的气体和液相浓度,由亨利定律描述:
在[X] X的平衡浓度是在溶液中(M =摩尔L”1),对二甲苯气相平衡压力(atm)和hx亨利定律常数(M atm-1)。表5.6显示了一些种类的一些值h兴趣溶解在水溶液25°C(施瓦兹,1984)。从~ f0 ~ 3 M atm——“相对不溶气体如02 ~ 105 atm-1等高度可溶气体H202 HNO,。
亨利定律适用于预测浓度的解决方案只有在某些条件得到满足。因此,
气相
气相扩散
气相
气相扩散
产品
图5.12示意图吸收和反应气体的液体。
蒸发
产品
图5.12示意图吸收和反应气体的液体。
表5.6亨利定律系数(H)的大气气体溶解在液体水25°C
气相
表5.6亨利定律系数(H)的大气气体溶解在液体水25°C
气体 |
H(摩尔L”1 atm ~”) |
参考“ |
o2 |
1.3 x三分 |
Loomis, 1928 |
没有 |
1.9 x三分 |
Loomis, 1928 |
c2h4 |
4.9 x 10 - 3 |
Loomis, 1928 |
没有/ |
1 x 10 - 2 |
施瓦兹和白色,1983年 |
啊, |
(0.82 - -1.3)x 10 - 2 |
布林和Perrottet, 1939 |
一氧化二氮 |
2.5 x 10 - 2 |
Loomis, 1928 |
有限公司/ |
3.4 x 10 - 2 |
Loomis, 1928 |
所以/ |
继续阅读:离子强度对速率常数
这篇文章有用吗?