从动力学
表5.2中的半衰期和一生的表达式可以方便地来源于速率定律。一阶反应污染物种类,反应的速率方程
- >产品是由
重新排列,这就变成了- d(一个)
整合从时间t = 0时的初始浓度是一个()时间t [A]浓度时,获得一个
一个半衰期后(即/ = t[/ 2)的定义
(一)= 0.5(一个)0。用集成率表达式,获得一个
二、三阶的反应,如果假设其他反应物的浓度比与时间常数,推导过程是一样的,除了k是取代/ c [B](二阶)或Jt [B] [c](三阶)。
但是在大多数实际情况下,至少另一个反应物的浓度不是恒定的,而是由于反应随时间变化,注入新鲜的污染物,等等。因此,使用半衰期(寿命)的污染物对第二或三阶反应是一个近似,涉及假定常数其他反应物的浓度。因此这些双分子的半衰期和三分子的反应直接影响其他反应物的浓度。
推导的速率常数k和r生命周期之间的关系遵循tl / 2,除此之外,从r的定义,在t = t [A] = [] 0 / e。
和氧化反应的S02 N02通过气相OH反应:
哦+ S02™H0S02 (fO)
的原因可以被依赖的三分子的反应压力反应(3)作为一个例子。放热债券之间形成0 (3 p)和02释放能量,必须移除形成一个稳定的03分子;如果能源仍然是内部能源,03年很快就会飞离而重新O + 02。第三个分子,M,是任何稳定的分子碰撞的兴奋(03)*中间,删除一些多余的内能。治疗反应(3)作为一个基本反应d [03]
率=莫][02][M] = +———dt有人可能认为利率增加第三体的浓度或压力M .然而,显然必须有一些限制因为速度不能增加到正无穷但只有一些上限取决于两个活性物种如何快速组合化学。结果,可以直观地预计,利率等反应(3),(10)和f (f)增加最初从零米的压力增加,然后在一些高原极限值在高压力。
让我们带哦的反应(10)S02大气关心的三分子的反应的一个例子并检测其压力依赖性。通常在动力学研究中遵循的衰败第二反应物过量反应物之一。的反应(fO),哦的衰变是跟随在S02过剩和第三身体M,其中M是一种惰性气体如他“浴”,
基于“增大化现实”技术,或者N2。因为它被认为是一个基本反应,反应的速率定律(10)可以写为低压力:
如果[M]是恒定的,[M]可以组合在一起,形成一个有效的双分子的速率常数,=
- - - = / c | q ' [0 h] [S02] [M] = *英尺[0 h] [S02]。
因为S02是多余的,其浓度即使变化不明显哦反应,因此它仍然是大约持续整个反应在其初始值,(二氧化硫)0。重排率法和积分时间t = 0时的初始浓度哦(哦)0时时间t浓度哦(哦),一个获得
自初始浓度哦,(哦)0,是一个常数,一块ln对反应时间t(哦)应该是一个直线斜率或衰变率由
衰变率(s”1) =二氧化硫]0。
这些衰变速率的阴谋反对(二氧化硫)因此0应该是线性的,与山坡上增加压力自k英尺取决于[M],
图5.1显示了这样一个情节的绝对值观察哦衰变速率对(二氧化硫)从50到402 0的总压力Ar托(阿特金森et al ., 1976)。正如所料,衰变速率是线性的(二氧化硫)0和M的压力增加。
得到三分子的速率常数的有效双分子的速率常数/ eft = / c |“[M]绘制在图5.2是总压强的函数(即。[M])。像预期的那样从前面的讨论中,/ eft增加[M]在低压力,但方法高原在更高的压力。
三分子的反应可以治疗,作为第一近似,就好像他们包括几个基本步骤,例如,对反应(f0),
哦+ S02 ^放送* (-12)HOSOf + M ^ H0S02 + M (13)
HOSOf是退出OH-SOz从债券形成加合物,包含多余的内部能量(12),和H0S02稳定加合物时产生的一些内部能量是通过碰撞与M。
如果系统被看作是精力充沛的浓度加合物(放送*)随时间保持不变,那么它的形成率和损失是相等的。这些利率可以写方程式。(12)、(-12)和(13)因为这是假定为基础反应。因此
——L。h = 0 = * [0] [S02] - * h (HOSOf)
这是稳态近似的一个例子,广泛用于气相动力学和机械的研究。
402年托202年托
100年托
50个托
402年托202年托
100年托
50个托
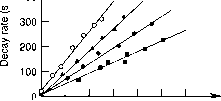
10“15厘米(S02) 0(分子”3)
图5.1块哦衰变速率与初始S02集中在基于“增大化现实”技术的总压力从50到402年托(改编自阿特金森et al ., 1976)。
10“15厘米(S02) 0(分子”3)
图5.1块哦衰变速率与初始S02集中在基于“增大化现实”技术的总压力从50到402年托(改编自阿特金森et al ., 1976)。
这篇文章有用吗?