Bioadsorbentsbased系统
目前关于生物吸附的综述涉及不同类型生物量的一般方法,如微生物生物量、植物废物和农业基废料,或特定的金属。494-98然而,关于利用大型植物生物量进行金属生物吸附的综述还没有。在本章中,综述了目前关于优先利用水生植物中无生命生物质进行生物吸附的知识。
生物吸附是活生物体和死生物体的一种特性,可以简单地定义为生物物质从溶液中去除物质。这些物质可以是有机的和无机的,也可以是气态的、可溶的或不溶的生物吸附已被证明是一种很有前途的从废水中去除金属的生物技术其主要优点是成本低,金属结合能力高,以环保的方式快速降低污染物浓度的效率高,简单,以及生物质的可用性93,99,100
Ahluwalia和Goyal94指出了生物吸附的一些缺点,例如生物质过早饱和,这可能是一个问题,因为在进一步使用之前,无论金属价值如何,金属解吸都是必要的。此外,生物过程改进的潜力是有限的,因为细胞没有进行活跃的代谢。
生物吸附是一个相当复杂的过程,受多种因素的影响,包括不同的结合机制(图10.4)。大多数负责金属结合的官能团存在于细胞壁中,包括羧基、羟基、硫酸盐、巯基、磷酸盐、氨基、酰胺、亚胺和咪唑基团。4,90植物生物量细胞壁含有蛋白质、脂类、碳水化合物聚合物(纤维素、木聚糖、甘露聚糖等)和Ca(II)、Mg(II)等无机离子。细胞壁中的羧基和磷酸基是直接影响生物质的吸附能力的主要酸性官能团
此外,对生物质表面进行化学改性以提高生物吸附性的研究已被广泛报道。用不同的模型描述了平衡91和动力学104。
近年来,基于不同类型的大型植物的生物吸附剂在文献中得到广泛的报道。免费的,漂浮的水生植物从Salvinia属,Azolla, Eichhornia, Lemna和Pistia被描述最多。在初始浓度为0.25 ~ 2 mg/L的低浓度As(V)条件下,沙蚕生物量对As(V)的吸收量分别为74.8%和54%;实验数据很好地符合Langmuir和Freundlich等温线。pH值和生物量量对吸附速率的影响也随一些代谢参数进行了研究
最近,无生命的cucullata生物量被认为是一种低成本的Cr(VI)吸附剂采用全析因法研究了经酸处理的黄瓜对Cr(VI)的最佳吸附条件。Cr(VI)的去除率adsorbent随时间、温度、吸附剂浓度和搅拌速度的增加而增大,随pH和吸附剂剂量的增加而减小。傅里叶红外光谱(FT-IR)分析表明,除静电力外,吸附可能是由于
-
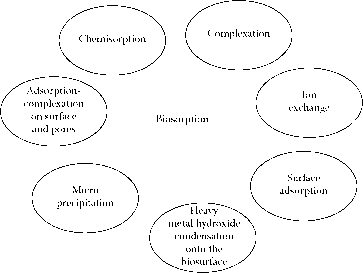
- 图10.4金属生物吸附中涉及的结合机制。
与吸附剂中的配体(Lewis碱)形成络合物。研究还显示了螯合作用的重要作用。作者认为,在低ph值下,螯合物的形成更容易,因此吸附效率更高。在最佳操作条件下进行柱状研究,获得的最大摄取量为98.75 mg/g。柱状研究的吸附数据很好地符合Bohart-Adams模型。此外,利用从胡参中提取的活性炭进行了去除Cr(VI)的研究。结果表明,吸附过程的初始阶段仅限于表面吸附,较慢的动力学可能是由于颗粒内扩散。FT-IR结果表明,该吸附剂与螯合物形成阴离子结合。还进行了柱状研究,以评价吸附剂处理Cr(VI)-的适用性被污染的水Cr(VI)在初始浓度为100 mg/L.107时,最大吸收量为156 mg/g
在不同阶段对Pb(II)、Cd(II)、Ni(II)和Zn(II)的吸附进行了评价。在NaOH和CaCl2/ MgCl2/NaCl的作用下,竹丝莲非生物生物量被激活。这一过程的发生是由于离子交换剂的增加,如(- coo)2Ca和(- coo)2Mg结合和/或- coona2ooc -基团。这些结合位点是果胶在碱溶液中去甲基化后与三元氯盐溶液接触形成的。在最高温度(313°K)下,碱处理生物量的qmax值较高,Pb(II)和Cd(II)的qmax值分别为1.272比0.977和1.35比0.931。这种生物量也有更快的吸附动力学相比,非活化的红蓝生物量
使用A. filiculoides非生物生物量也可以从水溶液中去除Hg(II)。多种技术,如扫描电子显微镜(SEM),氮和氨基酸含量的测定,BET (Brunauer, Emmett, Teller)在77 K的N2吸附表面积,酸/碱滴定,离子交换容量,电泳测量被用于试图阐明涉及汞封存的机制。样品与汞溶液接触平衡后,用能量色散谱和x射线衍射对其进行了表征。发现吸附剂表面Hg(II)还原为Hg(I),即可溶性汞还原为不溶性氯化汞(Hg2Cl2)是控制反应机理。虽然研究的汞吸附浓度与在工业废水,建议研究结果也适用于最后阶段水处理.109
较简单的技术已被报道用于研究生物吸附剂的酸性和碱性处理过程以及羧基和羧酸基在金属吸附中的作用。Rakhshaee和同事101使用电位滴定曲线来评估经NaOH和HCl处理的L. minor生物量中这些基团的含量。结果表明,naoh处理后的生物质对Hg(II)、Cr(III)、Cr(VI)和Cu(II)的吸附量增加(高达25%),这是- coo -基团(0.92 ~ 2.42 mmol/g)增加的结果。相反,-COOH基团增加(1.50 ~ 2.41 mmol/g),这是由于酸性处理导致金属离子吸收量下降(高达33%),尽管氯盐活化。
最近的报道指出,水葫芦(E. crassipes)无生命生物质适合开发一种高效的生物吸附剂,用于去除化学和相关加工工业废水中的铬。Gude和Das110发现,Cr(VI)在水溶液中的吸附速率符合一级动力学模型,且吸附平衡表现为langmuir型。Cr(VI)的最大吸附量为7.5 mg/g干重,而计算的活化能约为54.6 kJ/mol。在此基础上,作者提出,500mg左右的干生物质可以成功去除100ml含2.8 mg/L Cr(VI)的铬铁矿水中的Cr(VI)。相反,据报道,尽管拉格林雷竞技csgo一阶模型水葫芦生物量吸附Cr(VI)的部分数据适用,所有数据均适用拟二级反应模型。此外,发现Freundlich等温线能很好地代表所测得的吸附数据。FT-IR结果表明,在pH值1 ~ 5范围内,羟基是铬的结合位点,铬不析出。
中间螺旋体(spirrodela intermedia)、小螺旋体(L. minor)和分层螺旋体(P. stratiotes)能够去除Pb(II)、Cd(II)、Ni(II)、Cu(II)和Zn(II)离子,但前者的去除效率更高。数据只对Ni和Cd符合Langmuir模型,但对所有测试的金属都符合Freundlich等温线。吸附容量(KF)表明,铅在水中的吸附效率较高,S. intermedia和L. minor分别为166.49和447.95 mg/g。所研究的三种物质的吸附过程符合一级动力学。生物吸附的机制导致了一个离子交换过程存在于大型植生植物生物量中的作为反离子的单价金属与从水中吸收的重金属离子和质子之间
活化处理的效果也在多金属(Cu(II), Cd(II)和Ni(II))系统中进行了评估,使用未经处理的,酸预处理的(H2SO4)和碱预处理的(NaOH)生物质。结果表明,生物质在多金属体系中的吸附能力低于单金属体系,即未处理的生物质对Cd(II)的吸附下降了近60%。在多金属体系中,离子电荷、离子半径和电极电位影响金属离子的吸附。另一方面,碱预处理的生物质对Cd(II)、Cu(II)和Ni(II)离子的最大吸附容量更高(分别为83、69和59 mg/g)。FT-IR结果表明,干燥的生物质具有不同的与重金属离子结合的官能团,如羧基、磷酸盐、酰胺、硫醇和氢氧根
研究了E. crassipes、Valisneria spiralis和P. stratiotes非生物生物量对单金属和多金属水溶液中重金属(Cd(II)、Ni(II)、Zn(II)、Cu(II)、Cr(II)和Pb(II))的吸附能力。令人惊讶的是,V. spiralis是去除所有金属的效率最高的植物,E. crassipes是去除所有金属的效率最低的植物。螺旋弧菌对Cd(II)的去除率高达98%。Cr(II)、Ni(II)和Cd(II)的吸附数据更符合Langmuir等温线方程,Pb(II)、Zn(II)和Cu(II)的吸附数据更符合Freundlich等温线方程。总体而言,其他金属离子的存在对试验植物生物量的目标金属吸附能力影响不大。离子交换被证明是生物吸附的主要机制,在吸附的(H+和M2+)离子和释放的离子(Na+和K+)之间存在很强的离子平衡
对于沉水植物,狐尾藻(Myriophyllum spicatum L.)对Cu(II)的吸附速度快,符合Langmuir、Temkin和Redlich-Peterson等等温模型。对铜的最大吸附量(qmax)为10.80 mg/g,整个吸附过程用拟二级方程描述最好同样,海锥藻(Hydrilla verticillata)也被认为是一种很好的Cd(II)生物吸附剂。在批处理条件下,qmax计算为15.0 mg/g。此外,在连续流动研究中,轮孢水蛭生物量能够将Cd(II)浓度从10降低到0.02 mg/L以下的检测限值(固定床列)。还发现Zn离子影响Cd(II)的生物吸附
利用化学和仪器分析,包括原子吸收、电子显微镜和x射线能量色散分析,阐明了Potamogeton natans无生命生物量对Hg(II)的吸附机制。结果表明,整个生物质表面对Hg(II)的最大吸附量为180 mg/g。但表面有明显多层吸附Hg(II)的斑点。可以去除的溶液中Hg(II)的最低浓度约为4-5 mg/L.117
其他水生杂草,如芦苇草、红树(叶子)和睡莲(睡莲科植物)已被发现是有前途的去除铬的生物吸附剂。芦苇席对Cr(III)的吸附能力最强(7.18 mg/g),红树叶对Cr(VI)的吸附能力最强(8.87 mg/g),睡莲次之(8.44 mg/g)。值得一提的是,Cr(VI)在生物吸附剂上的单宁、酚类化合物和其他官能团的帮助下被还原为Cr(III),随后被吸附。与之前讨论的使用酸性处理的结果不同,在这种情况下,这种处理显著增加了生物吸附剂的Cr(VI)去除能力,而碱处理则降低了它
来自Parmelina和Cladonia属的地衣生物量对Pb(II)、Cr(III)和Ni(II)离子具有良好的生物吸附性能。采用Langmuir、Freundlich和Dubinin-Radushkevich (D-R)模型描述了巴美利亚科(Parmelina tiliaceae)生物量对Pb(II)和Cr(III)离子的吸附等温线。地衣对Pb(II)和Cr(III)离子的单层吸附能力分别为75.8和52.1 mg/g。D-R等温线模型表明,生物吸附是通过化学离子交换机制进行的自由能Pb(II)和Cr(III)的生物吸附分别为12.7和10.5 kJ/mol。计算得到的自由能(AG0)、焓(AH0)和熵(AS0)等热力学参数表明,在上述条件下,油油树生物量对Pb(II)和Cr(III)离子的生物吸附是可行的、自发的、放热的上述平衡、热力学和动力学模型也被用于描述叉枝枝孢生物量对水溶液中Pb(II)和Ni(II)离子的生物吸附。该生物质对Pb(II)和Ni(II)离子的单层吸附能力分别为12.3和7.9 mg/g。根据D-R模型,Pb(II)生物吸附的平均自由能为9.1 kJ/mol, Ni(II)生物吸附的平均自由能为9.8 kJ/mol,说明这两种金属离子的生物吸附都是通过化学离子交换机制进行的。与生物吸附能力相关的热力学参数表明发生了一个可行的、自发的、放热的过程。对实验数据也进行了动力学特性的测试,发现两种金属离子的生物吸附过程都遵循良好的伪二级动力学
最后,Chojnacka121研究了Riccia fluitans的生物吸附特性及其从水溶液中吸附Cr(III)的潜力。结果表明,该生物量蛋白质含量丰富(27 ~ 31%),具有较高的阳离子交换能力(14.5 mequiv/g)。羧基含量较高(6.08 mequiv/g)。此外,在多离子体系(Cu、Mn和Zn)中,由于金属离子竞争金属结合位点,Cr(III)的生物吸附能力显著受到影响(3.91 vs . 6.10 mequiv/g)。结果还表明,结合的金属离子与碱土金属发生了交换,证实了氟菌属结合金属的主要机制是离子交换。
正如本章前面所提到的,大多数生物吸附综述都涉及无生命生物量。然而,当代谢活跃时,使用活的生物量来理解各种生物吸附机制的存在也是相关的。S. minima已被证明是一种优良的铅生物剂。生物吸附过程遵循准二级动力学,并依赖于初始金属浓度(0.8 ~ 28.40 mg Pb/L)。数据很好地符合Langmuir和Freundlich模型。合成废水和去离子水的qmax值都很高(分别为58和44 mg/g)。如此高的吸附能力很可能是由于其特殊的物理化学特性,如非常高的表面积(264 m2/g)和良好的羧基含量(0.95 mmol H+/g干重)
研究发现,在自然条件下,白角藜(Ceratophyllum demersum)和Potamogeton pectinatus L.是Cd(II)、Cu(II)和Pb(II)的有效吸附剂。金属在植物表面的吸附率为Pb(II) > Cu(II) > Cd(II)。果胶柽柳生物量对重金属的吸附量高于白蜡柽柳。结果表明,这两个物种在污染水体的植物修复和生物监测研究中具有重要意义
在受控条件下,Lesage和合作者123评估了活的Myriophyllum spicatum生物量对Co、Cu、Ni和Zn的吸附/解吸特性。Co、Ni和Zn的吸附过程可以用Langmuir模型很好地描述,而Cu的吸附过程可以用Freundlich等温线模型更好地描述。生物质对Cu的亲和力最高,其最大吸附量为113 mg/g,分别是Co、Ni和Zn的49、38和17倍(分别为2.3、3.0和6.8 mg/g)。在最高初始浓度为100 mg/L时,铜在生物量表面的吸附量最高为29 mg/g。使用盐酸(0.1 M)也评估了生物质的潜在再生和重金属的回收。然而,酸洗并没有完全回收吸附在表面的金属,并且观察到生物质内部浸出的证据。因此,该手术不被认为是可行的策略。另一方面,Keskinkan和合作者124发现,使用M. spicatum活生物量去除Cu(II) (10.37 mg/g)和Zn(II) (15.59 mg/g)的qmax较低。与之相反,纹茅和白绒草对Pb(II)的qmax分别为46.49 mg/g和44.8 mg/g,具有较好的吸附性能。热力学参数,即具有负值的吉布斯自由能,表明了金属与植物之间吸附过程的自发性。铜和白绒草体系的该参数值最低(-0.45),铅和白绒草体系的该参数值最高(-10.83)。
10.5结论
植物过滤被定义为利用植物去除废水中的污染物,已被证明是一种高效和环保的生物技术。所有的植物过滤系统,如根过滤、水厂和泻湖,以及基于生物吸附剂的系统,在金属去除方面都非常有效。然而,选择合适的植物种类和/或特定的植物过滤系统对于在野外规模上的成功应用至关重要。水生植物,特别是自由漂浮和沉水植物,在这一领域显示出巨大的潜力。最后,即使大多数污染物的去除机制已经研究,更好地了解他们在一个特定的系统将是必要的增加植物过滤的成功应用案例。
参考文献
1.刘志刚,刘志刚,刘志刚,刘志刚。植物修复研究综述,植物科学进展,28(4):366 - 366,2005。
2.刘志刚,刘志刚,植物修复技术,植物科学进展,39(4),2005。
3.李丽英,李丽英,王志刚,植物重金属污染修复技术研究进展,环境科学学报,28(4),2007。
4.戴尔巴斯,刘志刚,重金属吸附在农业废弃物中的应用,环境科学学报,2004,26(2):528 - 528。
5.胡明辉,敖玉生,杨旭娥,李廷强,治疗富营养化水在深度流动技术系统中利用水生大型植物(iomoea aquatica Forsskal)减少养分,农业水管理,95,607-615,2008。
6.陈志伟,陈志伟,陈志伟,陈志伟,陈志伟,陈志伟,重金属废水的物理化学处理技术,化学工程学报,39(3),2006。
7.王志刚,王志刚,植物修复对生态系统重金属污染的影响,生态学报,30(5),666 - 666,2003。
8.Oliveira, w.e., Franca, a.s., Oliveira, l.s.,和Rocha, S.D,未处理的咖啡壳作为去除水溶液中重金属的生物吸附剂,有害物质杂志,152,1073-1081,2008。
9.王志强,李志强,李志强,小球藻生物修复技术的研究进展,生态学报,27(4),2008。
10.刘志刚,刘志刚,植物净化环境的研究进展,生态环境科学,4(4),2006。
11.鲍德温,P.R.,布彻,D.J,植物修复砷的两种超蓄能器水培环境科学与技术,2007,29(4):357 - 357。
12.杜申科夫,V. Kumar, N.P.B.A, Motto, H., and Raskin, I.,根过滤:利用植物去除水中重金属,环境科学与技术,29,1239-1245,1995。
13.杜申科夫,S.和Kapulnik, Y.,植物过滤的金属,在植物修复有毒金属:《利用植物净化环境》,拉斯金,I.和恩斯利,b.d., Ed. Wiley-Interscience,纽约,2000,第89-106页。
14.杜申可夫,李志强,植物修复技术的研究进展,环境科学,2004,27(1):1 - 7。
15.Verma, k.v., George, h.v., Singh, s.k., Singh, A., Juwarkar, A.和Singh, R.N.,模拟根过滤:植物根系对重金属的吸收,环境模拟与评估,11,387 -394,2006。
16.杨晓明,杨晓明,杨晓明,向日葵(Helinathus annuus L.) -一种具有环保产业潜力的作物,中国农业科学,30(6),457 - 457,2007。
17.牛志祥,孙丽宁,孙廷华,李玉生,王宏,向日葵、蓖麻、紫花苜蓿和芥菜对镉和铅的水培提取效果评价,环境科学学报,19,961-967,2007。
18.杨晓明,杨晓明,杨晓明,杨晓明,杨晓明,杨晓明,杨晓明,杨晓明,杨晓明,杨晓明,杨晓明,杨晓明,杨晓明,杨晓明,杨晓明,杨晓明,杨晓明,杨晓明,杨晓明,杨晓明,杨晓明,杨晓明,杨晓明,杨晓明,杨晓明。
19.Tandy, S., Schulin, R.,和Nowack, B., EDDS对水栽向日葵中重金属吸收的影响,化学杂志,62,1454 - 1463,2006。
20.Vonderheide, A.P., Mounicou, S., Meija, J., Henry H.F, Caruso, J. a ., Shann J. r .,基于HPLC-ICP-MS和esqtof - ms的芥菜根分泌物中硒含量的研究,分析杂志,131,33 -40,2006。
21.梅耶斯,D.E.R, Auchterlonie, G.J,韦勃,R.I,和Wood, B.,铅在芥菜根系统中的吸收和定位,环境污染,153,323 -332,2008。
22.莫瑞诺,安德森,C.W.N, Stewart, R.B., Robinson, B.H.,汞污染水的植物过滤:挥发性和植物积累方面,环境与实验植物学,62,78-85,2008。
23.杨晓娥,龙晓霞,叶宏斌,何志林,陈晓明,杨晓娥,高锌植物耐镉性和超富集特性的研究进展,植物生理学报(自然科学版),38(4):369 - 369,2004。
24.何斌,杨旭娥,倪文泽,魏玉芝,一种新的聚铅生态型景天属植物,植物学报,44,1356-1370,2002。
25.熊俊杰,何志刚,刘东东,杨晓霞,细菌在水介质中去除重金属的作用,化学工程学报,70,489-494,2008。
26.刘东,李廷强,金晓峰,杨旭娥,Islam, E, Mahmood, Q.,铅诱导植物生长和生长的变化抗氧化剂铅积累型和非铅积累型植物的代谢特征,植物学报,32(2),127 - 127,2008。
27.陈志伟,陈志伟,陈志伟,陈志伟,陈志伟,田菁(Sesbania drummondii)的铅富集特性研究,环境科学与技术,36(2),489 - 489,2002。
28.李志刚,李志刚,李志刚,杨晓明,杨晓明,田菁对汞的生理效应及其对水环境的影响,环境科学学报,29(4),591-598,2006。
29.刘志刚,刘志刚,刘志刚,植物去除水中铬的研究进展,环境科学与技术,29(4),457 - 457,1998。
30.王晓燕,王晓燕,王晓燕,王晓燕,王晓燕,植物对铅污染的修复研究,环境科学学报,29(1),39 - 44,2008。
31.李志刚,李志刚,李志刚,李志刚,李志刚。镉对两种盐生植物生长和矿物质营养的影响,植物生理学报,37(4),528 - 528,2005。
32.马丽清,张文华,蔡永明,杜春华,张文华,蔡永明,杨志强,杨志强,张志强,张志强,张志强,张志强,张志强,张志强。
33.马立强,杜淑娟,马立强,王志强,高砷聚砷蕨类植物对砷污染地下水的修复,中国环境科学,26(1),35-47,2004。
34.陈志伟,陈志伟,陈志伟,马立清,植物滤除对含砷地下水的影响,环境科学学报,28(3),2008。
35.艾尔斯,m.p.,波因顿,c.y.,威尔姆斯,c.a.,道尔,m.p.,洛佩兹,a.c.,索卡瑞,d.a.,弗格森,b.w.,布雷洛克,m.j.,植物过滤在新墨西哥州处理砷的中试规模示范饮用水,水科学,39,3863-3872,2005。
36.Srivastava, J., Kayastha, S., Jamil, S.,和Srivastava, V.,香根草的环境视角(L.)纳什。,植物生理学报,30,413-417,2008。
37.环境保护署(EPA)手册,人工湿地城市废水处理,EPA/625/R-99/010。可以在http://www.epa.gov/ORD/NRMRL2000一个。
38.美国环境保护署(EPA),人工湿地手册。可从http://获取www.epa.gov OWOW /湿地/ pdf / hand.pdf2000 b。
39.卡德莱克,R.,奈特,R.,维马扎尔,J.,布里克斯,H.,库珀,P.,和哈伯尔,R.,《污染控制人工湿地》。流程,性能,设计和操作,IWA出版社,伦敦,2000年。
40.美国农业部(USDA)人工湿地。可以在http://www.wsi.美国核管理委员会。usa.gov/ products/W2Q/AWM/docs / neh637ch3construct, 2002。
41.卢肖,范洛勒赫姆,范洛勒赫姆,戴波,N.基于模型的水平潜流人工湿地设计,水利学报,38,1484-1493,2004。
42.Wallace, S.,小规模人工湿地污水处理系统的可行性、设计标准和运维要求,IWA出版社,伦敦,2006。
43.Kandasamy, J.和Vigneswaran, S.人工湿地,新星科学出版社,纽约,2008。
44.Vymazal, J.和Kropfelová, L.,用水平分槽处理连续波废水表面流,施普林格,荷兰,2008。
45.杨晓明,王晓明,杨晓明。人工湿地中不同类型的营养物质的去除,环境科学学报,38(2),2007。
46.张晓霞,刘平,杨艳,陈伟,城市污水中观赏水生植物的修复作用,环境科学学报,19,902-909,2007。
47.格林威,M.,大型植物的作用营养物去除使用人工湿地,在环境生物修复技术,Singh, S.N.和Tripathi, r.d., Eds,施普林格,柏林,海德堡,
48.莱,p.k.,重金属污染水生生态系统湿地植物修复技术的研究进展,生态环境学报,2008a。
49.Miretzky, P., Saralegui, A,和Fernández Cirelli, A.,水生大型植物同时去除重金属的潜力(布宜诺斯艾利斯,阿根廷),Chemosphere, 57(8), 997- 1005,2004。
50.王晓明,王晓明,王晓明,王晓明,生物去除含铅废水的研究进展,环境科学学报,28(4),366 - 366,2008。
51.陈志明,陈志明,陈志明,王志强,王志强,水生蕨类植物对铅含量的影响,植物生理学报,34(4):366 - 366,2004。
52.王克生,黄丽春,李洪生,陈丕勇,张世辉,水培法萃取水中镉的研究进展,环境科学学报,32(4),666-672,2008。
53.Shukla, O.P, Dubey, S,和Rai,联合国,镉和铬的优先积累:混合金属处理下马齿草的毒性,环境污染与毒理学通报,78,252-257,2007。
54.Olguín, E.J., Vidal, M., Sánchez-Galván, G., and Houbron, E.,人工湿地对铅的吸附和细胞内积累因子:光照强度的影响,生物技术国际研讨会,中国大连,10月12-17日,
2008.
55.Choo T.P, Lee, C.K., Low, k.s.,和Hishamuddin, O.,利用睡莲(Nymphaea spontanea)从水溶液中积累铬(VI),化学学报,62(6),961-967,2006。
56.李志刚,李志刚,李志刚,黄志刚,黄志刚,黄志刚,黄志刚,黄志刚,黄志刚,黄志刚,黄志刚,黄志刚,黄志刚,黄志刚。
57.杨永平,李志刚,李志刚,杨志刚,铅和铬对水子叶的毒害作用,环境科学学报,26(1),39 - 39,2005。
58.Goulet, r.r., Lalonde, j.d., Munger, C., Dupuis, S., Dumont-Frenette, G., Prémont, S.和Campbell, P.G.C,铝冶炼厂废水的植物修复:含水生植物的介系中Al保留的研究,水科学研究,39,2291- 2300,2005。
59.李志强,陈志强,陈志强,植物对水体中重金属污染的影响,环境科学学报,28(3),366 - 366,2003。
60.Eapen, S., Singh, S.和D’souza, S.F.,金属和放射性核素的植物修复,在环境生物修复技术中,Singh, S.N.和Tripathi, R.D, Eds,施普林格,柏林,海德堡,2007,第189-209页。
61.李志强,李志强,李志强,黄志强,黄志强,黄志强,黄志强,黄志强,黄志强,黄志强,黄志强,2009。
62.Bragato, C., Brix, H.,和Malagoli, M.,芦苇中营养物质和重金属的积累(Cav.)指标。ex Steudel和Bolboschoenus maritimus (L.)威尼斯泻湖流域人工湿地中的帕拉,环境污染,144,967-975,2006。
63.崔俊华,朴世生,谢建荣,湿地沉积物中硫和微量金属的动态变化及其影响因素,环境科学学报,34(4),2006。
64.王晓燕,王晓燕,王晓燕,王晓燕。人工湿地污水处理对水体中铬的影响,环境科学学报,28(2),39 - 40,2008。
65.梅恩,M.A., Suñe, N.,哈达,H., Sánchez, G.,和Bonetto, C.,人工湿地植被对重金属和养分去除的影响,环境科学学报,90(1),355-363,2009。
66.Vymazal, J., Svehla, J., Kropfelová, L.,和Chrastny, V.,人工湿地和天然湿地中芦苇和Phalaris arundinacea的微量金属含量,环境科学,38(1),154-162,2007。
67.王晓明,王晓明,王晓明,湿地植物对重金属吸收、转运和释放的影响,环境科学学报,30(5),366 - 366,2004。
68.李志强,李志强,李志强,人工湿地在矿山酸性废水防治中的应用,环境工程学报,35(5),2009。
69.吴建生,何廷超,钱宏超,吴彦杰,林世明,庄仁华,水葫芦Cd- cd2结合物的研究进展,中国农学通报,29(4),589 - 589,2008。
70.李志刚,王志刚,王志刚,王志刚。镉和铅对羊草生长、生化指标和吸收的影响,环境科学学报,29(6),357 - 357,2008。
71.廖世伟,张乃林,水信子对人工湿地重金属污染的修复,水生植物学报,42,60-68,2004。
72.Olguín, E.J., Sánchez-Galván, G., Pérez-Pérez, T.,和Pérez-Orozco, A.,环境条件、EDTA和营养物质对微盐湖中铅的表面吸附、胞内积累和区系化的影响,工业微生物学杂志,32,577-586,2005。
73.Bennicelli, R., Stezpniewska, Z., Banach, A., Szajnocha, K.,和Ostrowski, J.,对城市废水中重金属(Hg(II), Cr(III), Cr(VI))的去除能力,化学学报,55,141-146,2004。
74.李志强,李志强,黄志强,黄志强,黄志强,黄志强,黄志强,黄志强,2008b。
75.陈志明,陈志明,陈志明,王志强,王志强,水生蕨类植物对铅含量的影响,植物生理学报,34(4):366 - 366,2004。
76.Olguín, E.J, Hernández, E.,和Ramos, I.,不同光照条件和pH值对Salvinia minima Baker去除镉、铅和铬能力的影响,生物技术学报,22,121-131,2002。
77.Sánchez-Galván, G., Monroy, O., Gómez, J.,和Olguín, E.J.,利用生物吸附和胞内积累因子评价盐渍草的超积累铅能力,水,空气,194,77-90,2008。
78.王晓明,李志刚,李志刚,杨晓明,镉和铅对盐渍草的毒害作用,环境科学学报,27(4),2006。
79.杨晓明,王晓明,杨晓明,杨晓明,铜对植物生理特性的影响,生态学报,44(1),47-56,2004。
80.刘志伟,刘志伟,刘志伟,刘志伟。热带城市污水生物滤除技术的研究进展,环境工程学报,30(4),2007。
81.王晓燕,王晓燕,王晓燕,王晓燕,采煤废水对水生态系统重金属污染的影响,环境科学与技术,29(5),2004,27 - 27。
82.刘志刚,刘志刚,刘志刚,刘志刚,刘志刚,刘志刚,刘志刚,刘志刚,刘志刚,刘志刚,刘志刚,刘志刚,刘志刚,刘志刚,刘志刚,等。
83.Jayaweera, m.w., Kasturiarachchia, j.c., Kularatnea, r.k.a.,和Wijeyekoon, S.L.J,水葫芦的贡献(Eichhornia crassipes (Mart.))不同营养条件对人工湿地铁离子去除机制的影响,生态学报,37(3),2008。
84.陈志伟,陈志伟,陈志伟,热带湿地生态系统的研究进展,生态学报,28(4),2006。
85.缅因州,M.A, Suñe, N,哈达德,H, Sánchez, G,和博内托,C,营养和金属去除在一个构造污水处理湿地冶金工业,生态工程,26,341-347,2006。
86.王志强,王志强,王志强,王志强,植物对含硒植物修复的研究进展,环境科学学报,28(3),366 - 366,2006。
87.王晓燕,王晓燕,王晓燕,王晓燕,王晓燕。湿地硫酸盐还原与锌固相的季节效应研究,生态学报,37(4),344 -344,2007。
88.陈志强,陈志强,陈志强,陈志强,植物对人工湿地水体中砷的影响,环境科学与技术,2009,29(2),457 - 457,2009。
89.Lesage, E., Rousseau, D.P.L, Meers, E., Van de Moortel, A.M.K, Du Laing, G., Tack, F.M.G, de Pauw, N.和Verloo, M.G,联合人工湿地处理生活污水的沉积物中金属的积累和芦苇生物量,水,空气和土壤污染,183,153 -264,2007。
90.加迪亚-托雷斯迪,j。l。德拉罗莎,G。和佩拉尔塔-维达。刘志强,王志强,植物过滤技术在废水处理中的应用,环境科学学报,37(4),2004,28 - 28。
91.加夫里列斯库,M.,生物吸附去除环境中的重金属,工程生命科学,4(3),219-232,2004。
92.Das, N., Vimala, R., and Karthika, P.,重金属的生物吸附-概述,印度生物技术杂志,7(2),159-169,2008。
93.盖德,G.M,生物吸附:对污染处理的科学原理、环境重要性和意义的批判性评论,化学技术与生物技术,84(1),13-28,2009。
94.王志伟,王志伟,王志伟,生物降解废水中重金属的研究进展,环境科学与技术,29(12),2004,27 - 27。
95.Mohan, D.和Pittman, C.U,使用吸附剂去除水/废水中的砷,评论,有害材料杂志,142(1-2),1- 53,2007。
96.吴志伟,王志伟,王志伟,王志强,植物废弃物吸附去除废水中重金属离子的研究进展,环境科学学报,2004,28(3):369 - 369。
97.南德,D.马哈詹,G.和考尔,mp .,农业废弃物一种新型吸附剂的研究进展,生物工程学报,39(4),457 - 457,2008。
98.李志强,杨志强,杨志强,生物吸附研究进展,生物工程学报,26(3),2008。
99.Freitas, O.M.M, Martins, R.J.E, Delerue-Matos, c.c.,和Boaventura, R.A.R,去除水溶液中的Cd(II), Zn(II)和Pb(II):动力学模型,有害物质学报,153,493-501,2008。
One hundred.古普塔,V.K.和Rastogi, A.,水旋藻物种对水溶液中铅的生物吸附:动力学和平衡研究,有害物质学报,152,407-414,2008。
101.刘志刚,刘志刚,刘志刚,刘志刚,林志刚,植物胞壁羧酸-羧酸比值变化对重金属去除的影响,环境科学学报,39(1),39 - 39,2009。
102.王志刚,王志刚,王志刚,王志刚,王志刚,王志刚,王志刚,王志刚,王志刚,王志刚,王志刚,王志刚,王志刚,王志刚,王志刚,王志刚,王志刚,王志刚,王志刚,王志刚,王志刚,王志刚。
103.巴沙,S., Murthy, z.v.p.,和Jha, B.,生物吸附六价化学修饰海藻铬的研究进展,化学工程学报,37(3),489 - 489,2008。
104.何玉生,赵文涛,徐春生,黄春涛,用蕨类植物作为吸附剂吸附水溶液中的铅离子,化学工程,33,55 -61,2004。
105.穆克吉,S.和库马尔,S.,水生蕨类吸附吸收砷(V)从水中,杂志水的供应科学通报,21(1),47-53,2005。
106.李志强,李志强,李志强,杨志强,杨志强,处理后水草对Cr(VI)的吸附机理研究,环境科学学报,28 (4),2008a。雷竞技csgo
107.王志强,王志强,王志强,王志强,王志强,热活化杂草对Cr(VI)的吸附,化学工程学报,2008b。
108.刘志刚,刘志刚,刘志刚,刘志刚,刘志刚,利用活性和活性氮杂唑去除水中Pb(II)、Cd(II)、Ni(II)和Zn(II)的动力学模型和热力学研究,环境科学学报,2004,29(1),39 - 41,2006。
109.Lloyd-Jones, p.j., Rangel-Mendez, j.r.,和Streat, M,螯合从水溶液中吸附汞离子交换树脂,活性炭和生物吸附剂,工艺安全与环境保护,82(4),302 -311,2004。
110.郭德明,李志强,杨志强,杨志强,水风信子对铬(VI)的吸附性能研究,环境科学学报,28(1),2008。
雷竞技csgo111.Mohanty K., Jha, M., Meikap, B.C,和Biswas, M.N, Eichhornia crassipes从水溶液中吸附Cr(VI),化学工程学报,117(1),71-77,2006。
112.Miretzky, P., Saralegui, A.和Fernandez-Cirelli, P.,死亡大型植物同时去除重金属的机制,化学杂志,62,247-254,2006。
113.陈志伟,陈志伟,陈志伟,陈志伟,陈志伟,陈志伟,镉(II)、铜(II)和镍(II)离子在基质中吸附的实验研究,环境科学学报,29(1),37 - 37,2005。
114.刘志强,王志强,王志强,王志强,植物生物量对重金属吸附的研究进展,生物工程学报,32(6),2003,32 - 38,2008。
115.杨春忠,王绍荣,曾爱云,金晓春,徐庆军,赵建忠,狐尾藻对铜的吸附动力学及平衡,环境科学学报,17(6),1025-1029,2005。
116.刘志刚,刘志刚,刘志刚,刘志刚,刘志刚,植物对镉吸附性能的研究进展,生物工程学报,37(6),2004,26 - 27。
117.李志强,李志强,杨志强,杨志强,植物对重金属的吸附研究,环境科学与技术,29(3),357 - 357,2002。
118.杨晓明,王晓明,杨晓明,杨晓明,水草对铬的吸附机理研究,环境科学学报,32(1),2008。
119.刘志强,李志强,李志强,李志强,黄志强,黄志强,地衣生物吸附Pb(II)和Cr(III)的研究进展,环境科学与技术,29(8),366 - 366,2008。
120.沙丽,杜泽,M, Uluozlu, O.D,和Soylak, M,苔藓(Cladonia furcata)生物质对水溶液中Pb(II)和Ni(II)的生物吸附,生物化学工程学报,37(2),151-158,2007。
121.王志强,王志强,王志强,黄志强,黄志强,黄志强,黄志强,黄志强,黄志强,黄志强,2007。
122.王志强,王志强,王志强,王志强,植物对水体中重金属和磷的吸附特性研究,环境科学学报,17(3),2008。
123.Lesage, E., Mundia, C., Rousseau, D.P.L, Van de Moortela, A.M.K, Du Lainga, G., Meersa, E., Tacka, F.M.G, de Pauwc, N.和Verloo, M.G,沉水水生大型植物Myriophyllum spicatum L.对工业废水中Co, Cu, Ni和Zn的吸附,生态工程,30,302 - 325,2007。
124.陈志伟,陈志伟,陈志伟,陈志伟,杨志伟,杨志伟,杨志伟,杨志伟,杨志伟,杨志伟,杨志伟,杨志伟,杨志伟,杨志伟,杨志伟,杨志伟,杨志伟,杨志伟。
继续阅读:pH对金属形态和毒性的影响
这篇文章有用吗?



