信息Tjz
温度(K)
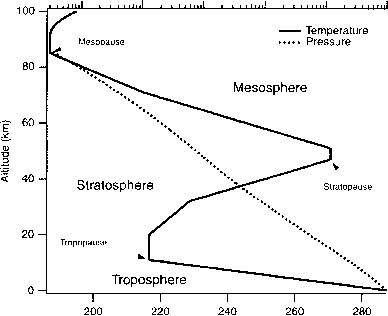
图1.1典型的温度和压力分布。基于1976年美国标准大气。
温度(K)
图1.1典型的温度和压力分布。基于1976年美国标准大气。
辐射会到达地面。O在吸收这些光子中的作用是至关重要的,因为250 nm波长的光子具有~5 eV的能量,足以破坏DNA中的化学键或以其他方式干扰生物过程[2^4]。
幸运的是,对于地球上的各种生命形式来说,O具有惊人的吸收波长在200到300纳米之间的辐射的能力。在250 nm处达到最大值吸收截面的O为1.15 x 10" cm2,在300纳米处下降到3.4 x 10 19 cm2(见DeMore et al.[5],表7)。为了了解Os作为吸收剂的有效性,我们可以估计辐射传输通过典型的常压柱,采用兰伯特-比尔指数吸收定律:
其中Tr是透射的入射光束的比例,a是0(在该波长(cm2)的截面,C是03的总柱丰度,通常在l()w个分子cm'2左右。在250 nm处,透射率为-10 50。这是一个小得惊人的数字,并表明基本上没有250纳米辐射入射到大气顶部,通过O,到表面。在300纳米处,O形截面相当小。大约3%的入射光束会到达表面。
对O的研究已成为公众感兴趣的主题,因为人们注意到,我们社会的排放可能会导致大气中O的含量逐渐降低。这种减少反过来又会导致地球表面的紫外线辐射增强,这对地球表面的各种生命形式是有害的。这本书中详细描述的许多研究都是为了更好地理解人类影响O,丰度的过程。关于()的早期研究历史,见Dobson[6|]和Nicolet[71。
O,也是气氛的重要组成部分,因为其他不太带有政治色彩的原因。其中之一就是O在平流层能量平衡中的作用。如上所述,O是一个巨大的紫外线光子吸收体。此外,O对红外线的吸收也很强,特别是在9.6 pm[8]附近。这种对太阳和红外辐射的吸收治愈了平流层,也是平流层温度随高度而升高的主要原因之一。
从年平均和全球平均来看,平流层大约在辐射平衡.O对太阳和红外辐射的吸收比O对红外辐射的发射多约15 W m2。因此,O是平流层的净热源。平流层的净加热被CO的净红外冷却所平衡,而H . o[9]。
平流层的O,也导致对流层-表面系统的净加热。太阳能吸收由平流层0;减少了太阳能向对流层-表面系统下降7w m \向下红外发射另一方面,平流层CO的红外发射增强使对流层-地面系统升温2w m,而H,0由于平流层温度升高使对流层-地面系统升温7w m。净效应使对流层-地面系统升温约2wm2[9]。因此,平流层O的消耗将倾向于使地表降温[10],尽管这种效应的确切大小和符号取决于O的高度,改变[11]。
O确实是平流层中一个重要的分子。因为它在平流层的许多方面都起着作用,所以要理解O,就需要对平流层的动力、化学和辐射过程有一个综合的看法。这种观点连接了传统的化学和物理学科,并象征着为了理解地球面临的问题而进行广泛思考的必要性。
1.1理想气体定律
在讨论0 "之前,我们先讨论理想气体定律,它与压强有关,密度和温度:
在平流层研究中,压力通常以百帕(hPa)或毫巴(mb)表示,它们是等效单位,例如1 hPa = 1 mb。压力有时也以torr表示(1 torr = 1.3332 hPa)。然而,当使用理想气体定律时,压力通常必须转换为MKS单位帕斯卡(Pa;1 Pa = 0.01 hPa = 1 kg m s 2)。温度总是以度开尔文(K)表示。所使用的常数决定了密度的形式。如果常数是通用气体常数(R = 8.31 J mol1 K '),则密度单位为摩尔每立方米(mol ' m ')。如果常数是气体恒定为干燥空气(R = 287 J kg 1 K ')则密度单位为千克每立方米(kg m ')。最后,如果常数是玻尔兹曼常数(k = 1.38 x 10'23 J分子1k '),那么密度就是分子每立方米,也就是数密度。很明显,确保方程中的单位是一致的是至关重要的。如果做不到这一点,可能会导致几个数量级的错误,让你在同事面前看起来很愚蠢。相信我。
平流层研究中最常用的密度形式是数密度,几乎总是以每立方厘米分子为单位。如果理想气体定律中使用的压强是气体的分压,那么确定的密度将是特定气体的密度。组成X的数密度(X = 02, N>, of, 11,0等)一般记为[X)。如果在理想气体定律中使用总压力,则确定总数密度,记为[M]。在化学方程中,我们也用M来表示“任何分子”,而不考虑其元素组成。实际上,这意味着M指的是N2和02。计算数密度的一个有用的简便方法是,压强P是X的分压,单位是百帕,温度T是开尔文。若P为总压力,则计算总数密度[M]。注意个体的数量密度之和大气成分和必然等于总密度,就像分压之和必然等于总压一样。
表示一种成分丰度的另一种有用的方法是体积混合比(VMR)。从概念上讲,组成X的VMR是给定体积中X分子的比例。从数学上讲,VMR是X的数密度与总数密度的比率:[Xj/IMJ。vmr是无因次压力=常数x密度x温度
由于VMR通常很小,通常乘以10h, 10”或1()12即可得到百万分之一体积(ppmv),十亿分之一按体积(ppbv)或按体积(pptv)计算的万亿分之一。例如,VMR为5 x10 6或5 ppmv的O,意味着样品中每1x10英寸(或每200,000个)分子中有5个是O分子。最后,一个气团中所有成分的vmr之和必须等于1。
VMR为什么有用?设气压为P0,温度为T "时空气中X的密度为[X] "。现在假设空气块移动到大气中的一个新的位置,温度和压力变化到和T1KV。根据波义耳定律和查尔斯定律,X的数密度为
现在考虑VMR。X的初始混合比为[XJu/lM]…,其中[MJ”为初始总数密度。新温度压力下的VMR为[X|mrw/|Ml " ew,其中[X|,ll lv由式1.4和给出
结合式(1.4)和式(1.5),新位置的VMR为
因此,当一个气团中的温度或压力变化时,一个成分的数量密度变化,VMR不变化。换句话说,VMR对于包裹的压力或温度的变化是守恒的。这个属性使得VMR非常有用。值得注意的是,人们也可以定义质量混合比(见本章末尾的问题4),但这在平流层研究中很少使用。
1.2臭氧形态
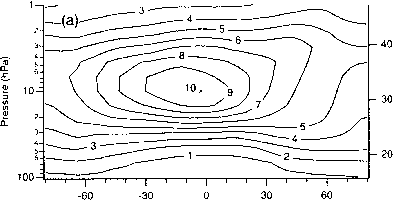
图1.2显示了在i -tude-height平面上,O的数密度和VMR的等高线。O,在赤道上的数密度(4.6 x 1012分子厘米'在-25公里处)和VMR (10 ppmv在-32公里处)均达到最大值。当一个人远离赤道时,数字密度峰值移动到较低的高度,但是
-
- 纬度
继续阅读:K
这篇文章有用吗?
