海水和海洋沉积物中的氢和氧同位素
现在我们将把注意力转向水和从水柱中沉淀下来的沉积物中所含的氢和氧的同位素。我们将了解这些同位素的浓度如何告诉我们冰川的体积和海洋各个部分的温度。“正常”的水是H2l6O,但氢或氧的其他同位素可以替代最常见的同位素,导致各种形式的重水,特别是HD16O和H28O。
^轻水和重水
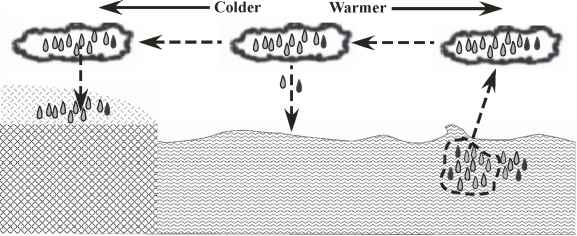
图1.5:显示陆地上冰盖的增长如何影响海水的同位素组成的草图。从海洋中蒸发的水蒸气富含较轻形式的水,并且随着较重形式的水在剩余的水沉积在冰川上之前先雨雪排出而变得同位素更轻。这个过程系统地将同位素轻的水转移到冰川,留下同位素重的海洋。
图1.5:显示陆地上冰盖的增长如何影响海水的同位素组成的草图。从海洋中蒸发的水蒸气富含较轻形式的水,并且随着较重形式的水在剩余的水沉积在冰川上之前先雨雪排出而变得同位素更轻。这个过程系统地将同位素轻的水转移到冰川,留下同位素重的海洋。
在任何给定温度下,轻分子的平均运动速度都比重分子快。这意味着在蒸发过程中,较轻的同位素形式水蒸发比较重的形式更容易,导致蒸汽在轻水中富集,在重水中相对于液体储层而消耗。此外,当水蒸气凝结成液体或冰时,较重的形式更容易凝结,因为运动较慢的分子更容易粘在一起而不会相互反弹。因此,相对于空气中的蒸汽,降雨以重形式富集,而留在空气中的蒸汽以轻形式进一步富集,以重形式进一步消耗。这是蒸馏的一种形式,非常类似于用葡萄酒酿造白兰地(或用发酵的玉米醪酿造私酿烈酒)的过程。酒精比水更容易挥发,因此与加热后的葡萄酒接触的蒸汽相对于液体的酒精含量更高;如果部分蒸汽冷却并冷凝,水优先冷凝,如果其余蒸汽分别冷凝,则在蒸馏器的末端留下强有力的精华。
蒸馏过程影响海水同位素组成的方式如图1.5所示。让我们假设海洋以相对于VSMOW为零的ó18O开始。水会蒸发到空气中,直到空气中充满水蒸气为止(这个概念将在第二章中详细说明)。由于重分子比轻分子不易蒸发,因此相对于海洋,水蒸气在18O时就会消耗殆尽——换句话说,它将是同位素轻的。更准确地说,空气中水蒸气的18O与16O之比将小于原始海水的比例,导致蒸汽的S18O为负。耗竭量与温度的关系不大。273K时,水蒸气
S18O
相对于海洋的位移为-11.7。在290K时,位移为-10.1%,在350K时,位移为-6.0%。随着温度升高,储层间同位素对比的减少几乎是所有储层的典型特征同位素分馏问题。因为水的存储量的形式大气中的水蒸气与海洋里的水量相比是微不足道的,对轻同位素的选择性去除使得海洋的同位素重量非常非常轻。但是,如果我们将大气中的水蒸气移走,将其封存在陆地上的冰川中,并多次重复这一过程,直到相当一部分海水转变为同位素含量较轻的冰川呢?在这种情况下,从海洋中系统地去除大量同位素轻的水将使海水的同位素重量显著增加——它将具有显著的正S18O。因此,海洋中同位素重水的富集程度告诉我们陆地上已经形成了多少冰。当冰体积变大时,剩余海水的S18O(或类似的SD)变得更正。举个例子,假设我们从平均深度为4公里的海洋中移走200米深的水来建造冰盖,假设冰川是由S18O = -10%o的蒸汽建造的。如果Sj是冰的S18O,海水的S18O也是,那么分子守恒意味着200Sj + (4000 - 200)So = 0,如果海洋开始时S18O = 0。由此得出So = .526%o。
事实上,由于图1.5中所描述的原因,最终降雪形成冰川的水的同位素含量要比仅仅观察与海水平衡的蒸汽所预期的-10值轻得多。最初水分蒸发。蒸汽可能有S18O = -10,但在前往寒冷的极地地区的途中,一些水会像雨一样回到海洋中,而凝结水相对于蒸汽的同位素重,因为重的物质更容易凝结。这意味着每当一些大气中的水蒸气因降雨或降雪而流失回海洋时,留下的蒸汽就会变轻。当雪最终落在冰川上时,额外的闪电的确切程度取决于途中失水的量,而失水又是从海洋中吸收的水和在冰川上落下的水之间的温差的函数。在过去的10万年里,格陵兰岛降雪的S18O值从最冷时期的-42到今天的-35%左右不等。南极冰的同位素比格陵兰冰轻一些,S18O值在-40到-55之间,这取决于冰的位置和年龄。由于在到达极点的过程中发生了额外的分馏,冰川的形成将使海洋中重同位素的含量比我们之前估计的要丰富得多。对于同位素组成与现在的冰川相当的冰川来说,移除200米的海洋来建造冰川将使海洋的碳含量增加约2%,而不是仅仅增加0.526%。前面的讨论还表明,为了将海洋的S值转换为冰体积,人们需要对正在形成的冰川的同位素组成进行一些估计。对于现在的冰川,这可以通过在冰层上钻孔来确定,但对于过去已经不存在的冰川,人们必须依赖于建模。
所以,如果我们能回到过去,拿起一桶海水,测量它的同位素组成就能告诉我们地球上冰的体积,这就能告诉我们地球有多冷。如果有办法做到这一点岂不是太好了?
在现实中,同位素水的组成海洋上方大气中的水蒸气在某种程度上偏离了平衡值,因为水蒸气处于海洋蒸发和高空干燥空气混合之间的动态平衡状态。只有当空气中充满了水蒸气时,空气才会变得湿润平衡分馏适用于完全。
-

- 图1.6:死去底栖有孔虫(Cibicidoides Robertsonianus)的壳。标本的直径约为1.5毫米。
这篇文章有用吗?
