光化学
吸热反应的进一步例子包括光化学反应.在这种情况下,吸热反应进行所必需的额外能量来源是太阳辐射,它可以破坏大气物种的化学键。在本书中,我们只考虑其中之一光化学过程: photodissociation.1
物理更新太阳辐射组成电磁波.电磁辐射具有双重波粒性质。这意味着电磁辐射同时具有波状和粒子状的性质。在其波形中,电磁辐射可以被认为是一组叠加波,有时被称为在真空中以光速c = 2.998 x 108 m s-1传播的集合,与波长无关。这个集合中的每个波都可以被视为具有特定波长、频率和振幅的简单正弦函数(见图8.1)。波长X是波的两个连续波峰之间的距离。X的单位是米。波的频率,f,是一秒钟内通过观察者的周期数。频率的单位是赫兹(1hz是每秒一次振荡)。单个波的波长和频率的乘积等于光速(速度是距离除以时间):c = X X f。从这个方程可以看出,频率较高的波具有更短的波长,频率较低的波波长较长。
当辐射与原子或分子相互作用时,它只能被某些离散的能量所吸收或释放。换句话说,电磁辐射是量子化的。波可以被认为是一束被称为光子的粒子,它携带着离散的数量或能量包。光子的能量
1感兴趣的读者可以参考Peter V. Hobbs(2000)的《大气科学基础物理化学》以获得更多关于光化学反应的信息。
-
- 102
可见(400-700 nm)
伽马射线
x射线
紫外线
红外
微波
无线电波
10 14 = 10-5nm 10 - 13 = 10 ^ nm 12 = 10-3nm 10 - 11 = 10-2nm 10 - 10 = 10 - 1 - 9 = 1 nm换= 10 nm 10 - 7 = 100海里10 - 6 = 1结果|我的纯= 10 4 |我打败= 100 |我“三分= 1毫米霁
图8.2电磁波谱.
频率f为
其中h是普朗克常数,h = 6.62 x 10 -34 J s。如果我们用x表示f,我们得到hc
因此,波长越短(频率越高)的光子能量越大。从无线电波到伽马射线的电磁波谱如图8.2所示。能量最大的光子是伽马射线。当一个人从伽马射线垂直向下移动到无线电波时,能量会减少,频率也会减少,而波长会增加。光谱的窄带对应于可见光。可见光范围内的光子(大约400-700纳米)可以被人眼探测到。紫外线的波长比可见光的波长短(频率高)。
为了描述穿透大气层的辐射,引入能量通量的概念是有用的。能量通量(能量通过单位面积垂直于光束,每单位时间)由
其中n0是单位体积的光子数(气体中的光子数密度)。太阳光子在大气顶部的能量通量为1370 W m-2。这个参数叫做太阳常数。通过大气传播的太阳光子可以被大气成分吸收和/或散射。考虑在波长X处由于光子吸收造成的光子通量衰减正常的发病率为简单起见(太阳在天顶,正上方(图8.3))。我们把波长X处的光子能量通量记为FX;它的维度是单位面积的能量,单位时间的能量,单位波长的能量。如果在大气顶部,单位波长的通量为FX(top),则高度z的通量FX(z)用
Fx(z) = Fx(top) exp(-r(z))[垂直太阳光束的衰减]。(8.12)
投资策略基金会(上)
图8.3原理图一束从头顶直射而来的太阳光束,其强度的衰减用阴影表示。
这个方程是由辐射转移理论推导出来的。2在指数半径上的系数t称为光学深度:
光学深度t与垂直积分柱密度f™N (z)dz成正比,其中N是在x处吸收的大气物种的浓度。从z到to的积分反映了光子从大气顶部传播到高度z的路径。比例系数a称为吸收截面.这个参数描述了特定气体种类吸收光子的能力;它的测量单位是m2(在文献中通常是cm2)。吸收截面可以在实验室中测量。当光学深度接近于单位时,通量衰减了大约3倍(e ~ 2.7)。例如,X在240 - 300 nm(紫外范围)之间,由于臭氧在30-38 km高度的吸收,t达到单位。这意味着在这个范围内的太阳光子会被平流层中的臭氧吸收,而不会到达对流层。波长较短,在175至200纳米之间,辐射在40至80公里的高度被氧气吸收。在波长大于310纳米时,大多数光子穿透对流层并到达表面。如果太阳天顶角0 = 0,则通量衰减公式中必须加上cos 0(图8.4):
Fx (z) = Fx (top) exp(-t(z)/cos 0)[天顶角0的衰减]。(8.14)
天顶角越大,在给定高度z处衰减越强。
紫外线和可见光范围内的光子具有足够的能量将分子分解。这个过程叫做光解作用。光解离在对流层和平流层中起着非常重要的作用。例如,对流层中的一个关键反应是臭氧通过紫外线辐射光解离:
其中,符号hf表示频率为f的光子。这个符号强调光子携带的能量是频率乘以普朗克常数。对流层臭氧的形成是由于NO2的光解作用:
光束在距离间隔dz中衰减的量与入射光束的通量和间隔中衰减物质的量成正比。结果是dFx = -AFx dz,其中A与单位体积衰减物质的量成正比。这个方程的积分会导致沿路径的指数衰减,被称为比尔定律。
-
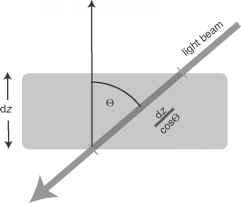
- 图8.4太阳光束从右上方穿过厚度为dz的物质板示意图。平板中的路径长度为dz/ cos©,其中©为太阳天顶角。
然后,原子氧与O2重新结合,形成臭氧:
臭氧层的形成也是由光解作用引起的。在平流层中,X < 240 nm的紫外线辐射会光解分子氧O2,产生原子氧:
然后由原子氧和分子氧的重新结合(反应(8.17))形成臭氧。
例8.3考虑一个氧分子的光解作用产生两个基态氧原子:
反应进行需要多少光子能量?电磁波谱的哪一部分对应这个能量?
答:首先让我们看看标准焓关于这种反应:
AH°= 2 × 249.17 - Na hf = 498.34 kJ mol-1 - Na hf (8.20)
NA是阿伏伽德罗常数。为了找出打破一个O2分子所需要的光子的最小能量,我们必须使这个反应的标准焓等于零。只有能量hf大于这个最小能量的光子才能将O2分子分开:hf > 498.34/NA kJ。这个不等式给出了所需的最小频率值:f > 498.34 x 103/(6.022 x 1023 x 6.62 x 10-34) = 12.49x 1014 Hz,或最大波长。X < 0.24x10-6m = 240 nm。因此,反应(8.19)的进行需要X < 240 nm的辐射,它对应于光谱中的紫外线部分。□
如果我们知道化学键的解离能,我们就可以在不考察焓的情况下求出某个反应进行所必需的光子能量。
在白天,平流层中NO的一个重要来源是NO2分子的解离:
如果NO2分子的解离能为5.05 x 10-19J,求出该反应所需的最大电磁辐射波长。离解能通常以电子伏特:3表示
1电子伏(eV) = 1.6 × 10-19J (8.22)
(这种反应在被污染的城市空气中也很重要,因为它是对流层臭氧的来源之一)。
解离NO2分子需要能量为hf > 5.05 x 10-19 J的光子。那么,f > 5.05 × 10-19/(6.62 × 10-34) = 7.6 × 1014 Hz。最后,X < 2.998 X 108/7.62 X 1014 = 0.39 X 10-6m = 390 nm,处于光谱可见光和紫外部分的边界。□
继续阅读:热力学方程
这篇文章有用吗?
读者的问题
-
劳拉2个月前
- 回复




