列举5种可能存在于废硬水中的溶质
0.005 Mc5h7no2 0.005 -113 g mol-1 C5H7O2N Mno2-n 14 g mol-1 NO2-N
g MLVSS
生长时不积累NO-的总产量值亚硝化单胞菌而且硝化菌属每氧化1克NH4-N或产生1克NO3-N, MLVSS为0.187克。Lindemann(2002)和Choi(2005)提出并比较了一些屈服系数。YXA/NH4-N和YXA/NO2-N的平均值由不同作者的值计算得到(Larsen-Vefring 1993):
Yxa/n02-n = 0.02 ~ 0.084 = 0.048 g MLVSS (g NO2-N)-1
这里的总参数MLVSS(混合液体悬浮固体)分别只包括亚硝基单胞菌和硝酸杆菌的质量。
衰变率(死亡率和死亡率)的影响内源呼吸)没有被考虑。硝化菌生长与耗氧量的产氧量系数计算如下:
YXa/ nhh n 0.147 g MLVSS = Ixa/nH4-n =-= 0.043—(10.20)
YO2/NH4-N 3.43 g O2
YXA/NO2-N 0.04 g MLVSS
Yxa/O2 = = - = 0.035 (10.21)
从产氧量系数可以看出,硝化反应的特点是耗氧量高,生物量低。从方程式。(10.20)和(10.21)可以看出,亚硝基单胞菌和硝酸杆菌的细胞增殖所用的氧气几乎相同。
氨和硝酸分别被认为是亚硝基单胞菌和硝酸杆菌真正的电子供体(底物),因为与NH+或NO-等电离分子的运输相比,氨和硝酸运输进入细胞所需的能量更少(Suzuki et al. 1974;Bergeron 1978;Wiesmann 1994)。NH3和HNO2是由解离反应形成的,解离反应可以用解离平衡来描述pH值和温度:
Nh + (1 > nh3 + h + (10.22)
No - + h + <»hno2 (10.23)
NH3和NH+的浓度可由解离常数KD表示,NH3 = k2/k1由式(10.22)表示:
Kd,nh3 = s Snh+'ns (10.24)
:
SNH4-N + SNH3-N = SNH4-N,x (10.25)
将Eq.(10.25)引入Eq.(10.24)得到:
Snh4-ni - snh3-n (10 26)
S = Snh4-n^ (10.27) SNH3-N= 1 + Kd,nh3 '10-ph
地点:
pH = -logSH+;SH + = 10-pH
注意,SNH+_N>2与SNH+-N在6.0 < pH < 7.8(通常废水处理的pH范围)时大致相同。最后,这导致(Anthonisen et al. 1976;Wiesmann 1994):
NH3_N 1 + Kd,nh3 -10_pH与:
6344
HNO2-N浓度的计算方法类似:
:
Kd,HNO2 = exp i_ 273+T1 (10.31)
-
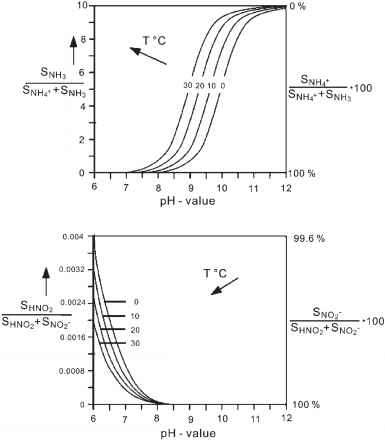
- 图10.3温度和pH值对NH3和HNO2解离平衡的影响
NH3/NH+ + SNH4和HNO2/NO- + SHNO2的解离平衡温度和pH值如图10.3所示。
认识到SNH3随着pH的增加而增加,而SHNO2随着pH的增加而减少是非常重要的。
提出了一种基于霍尔丹动力学的硝化反应动力学描述。这两个方程都适用于富含铵和亚硝酸盐的废水,其中铵和亚硝酸盐氧化都受到底物过剩的抑制(见式10.32和式10.33)。
P-NS = P-maxNS '——' ~rp-"(1°.32)
SNH3-N kns +c
pNB = pmax,NB ' - s2 - ' K ' +c ' (10.33)
ç SHNO2-N KNB + c
对于较高的Snh3-n(较高的pH值)或Shno2-n(较低的pH值),反应被抑制。
对于较低的Snh3-n或Shno^n,例如在城市污水处理厂,根据霍尔丹动力学的抑制可以忽略不计。c 'P K'可忽略氧限制。根据这些假设,等式。(10.32)和(10.33)的结果是简化的动力学描述,分别用于低氨和低亚硝酸盐浓度的污水处理厂的硝化:
PnB = Pmax,NB ' ~ ~ (10.35)
表t0.3给出了硝化动力学系数和产率系数。
通常情况下,铵氧化亚硝酸盐被认为是硝化制硝的瓶颈。但在低pH、低c′和低温条件下,NO-的氧化速率明显低于NH+。可以观察到NO积聚(见第10.2.4节)。如果NH+只被氧化成NO-, NO-随后被反硝化,则是有益的生物脱氮系统。通过亚硝酸盐途径脱氮也是一种环境更清洁的工艺,降低了曝气和碳源的成本(例如,甲醇作为电子供体)。此外,据报道脱氮率亚硝酸盐比硝酸盐快1.5-2.0倍(Abeling和Seyfried 1992)。通过亚硝酸盐积累脱氮的概念将在第10.2.4节中详细解释。
如果在有机物浓度较低的废水中添加CO2作为碳源,导致低CO2的形成,其浓度可能是一个速率限制因素,特别是如果高浓度的NH+在pH值较高的地区被氧化(Green等,2002年;Carrera et al. 2003)。
表10.3自养硝化动力学系数和产量系数。
参考T ^maX KNh”。n Kw K' YXa/n"1
(°C) (h1) (mg L-1 N) (mg L-1 N) (mg L-1 O2)
诺尔斯等人(1965) |
30. |
0.0822 |
0.084 |
- |
- |
- |
Bergeron (1978) |
25 |
0.0064 |
0.138 |
35 |
1.8 |
- |
Nyhius (1985) |
15 - 17日 |
0.04 |
0.056 |
33 |
0.5 |
- |
东布罗夫斯基(1991) |
20. |
0.0138 |
0.714 |
540 |
0.29 |
- |
Wiesmann (1994) |
20. |
0.032 |
0.028 |
540 |
0.3 |
0.147 |
霍恩和亨佩尔(1996) |
20 - 22 |
0.0063 |
0.5 |
- |
0.5 |
0.062 |
Pirsing (1996) |
25 |
0.038 |
0.03 |
200 |
0.3 |
0.142 |
林德曼(2002) |
22.5 |
0.0074 |
0.079 |
16.5 |
0.25 |
0.142 |
NO2氧化 |
||||||
诺尔斯等人(1965) |
30. |
0.058 |
1.9•10-4 |
- |
- |
- |
Bergeron (1978) |
25 |
0.005 |
2.5•10-4 |
35 |
1.4 |
- |
Nyhius (1985) |
15 - 17日 |
0.016 |
1.7•10-4 |
0.15 |
0.75 |
- |
东布罗夫斯基(1991) |
25 |
0.019 |
0.39•10-4 |
0.25 |
1.1 |
- |
Wiesmann (1994) |
20. |
0.045 |
0.32•10-4 |
0.26 |
1.1 |
0.042 |
Okabe et al. (1995) |
20. |
0.034 |
0.94•10-4 |
- |
0.68 |
0.083 |
Pirsing (1996) |
25 |
0.041 |
0.55•10-4 |
0.1 |
1.3 |
0.048 |
林德曼(2002) |
22.5 |
0.019 |
3.0•10-4 |
0.26 |
1.27 |
0.048 |
a) NH4氧化:g MLVSS (g NH4- n)-1;NO2氧化:g MLVSS (g NO2- n)-1。
a) NH4氧化:g MLVSS (g NH4- n)-1;NO2氧化:g MLVSS (g NO2- n)-1。
10.2.2.3影响硝化的参数
有几个参数影响硝化细菌种群进行硝化的能力,如c', pH, T, tR和T ^。在所有这些参数中,c'和pH是最重要的。
硝化细菌是严格的需氧菌.如果没有氧气供应,硝化速率完全受限。式(10.32)和(10.33)显示了氧气对硝化速率的影响。例如,可用KNb = 1.1 mg L-1 O2估计氧限制区域(见表10.3)。极限点可以给出为p = 0.9 pmax(最大生长速率的90%),在c’= 9.9 mg L-1 O2时已经达到(另见式6.11)。这意味着在空气曝气时,氧气浓度对硝化速率总是有限制作用。
为了进行有效的硝化作用,应监测曝气池中保持的c'量作为控制参数,以确保NH+、NO-和NO-的永久流出浓度。过曝气的做法是昂贵的,甚至可以有助于硝化细菌絮凝体的剪切和/或提高泡沫的产生。
生长速率与pH值之间的关系由等式给出。(10.28)和(10.32)的铵氧化和等式。(10.30)和(10.33)亚硝酸盐氧化。的最佳pH值对于硝化细菌的生长,通常假设pH值为7.2-8.0,取决于SNH4(见式10.28)。如果曝气池的pH值低于pH 5.5或高于pH 9.0,由于蛋白质损伤,硝化作用会显著降低。一个低废水pH值是否有抑制硝化菌酶活性的主要作用二次效应关于碱度的可用性。
温度的下降导致硝化细菌的生长速度显著降低。一些作者(霍普伍德和唐宁1965;诺尔斯等人,1965年;Painter和Loveless 1983)描述了硝化作用的温度依赖性。为了描述温度对硝化和反硝化的影响,我们使用生化反应的Arrhenius方程(见式3.1)。
在硝化过程中最大生长速率的温度依赖性已经由Knowles et al.(1965)发表:
Pmax。n = 0.042 exp(0.0351T-2.174)NB = 0.042 exp (0.0587T-1.13)
硝化速率是温度在8°C和30°C之间的函数。冬季废水温度过低会对硝化产生不利影响。因此,温带地区的许多监管机构根据季节有不同的氨排放限值。
图10.4显示了硝化细菌生长速率随pH值和温度变化的最佳硝化范围(Larsen-Vefring 1993)。
低温、c'和/或极端pH值的短暂和长期下降会导致不完整的硝化作用这会导致操作中断。
-
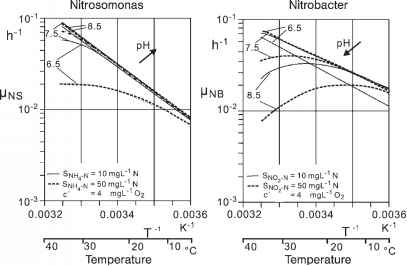
- 图10.4硝化细菌的比生长速率与pH和温度的关系(Larsen-Vefring 1993,计算)。
参数 |
最佳范围/值和注释 |
c ' |
2-3 mg L-1 O2, c'限制硝化作用 |
PH值 |
pH 7.2-8.0, pH <5.5, >9.0临界 |
温度 |
T = 28-32°C, T <5°C和>40°C临界值 |
SNH3 |
抑制亚硝基单胞菌>10 mg L-1,硝化杆菌>0.1 mg L-1 |
SHNO2 |
抑制亚硝基单胞菌和硝基细菌>1.0 mg L-1 |
SNH4 |
抑制硝化> 400-500 mg L-1 |
硫氧还蛋白 |
> 4-6天,随降低温度 |
tR |
>低温10h |
X |
> 2 g L-1 MLVSS |
FMa比值) |
~ 0.5 g NH4-N (g MLVSS)-1推荐 |
表10.4总结了有利于硝化的操作参数。一般来说,增加T、tR、SN和足够高的T ^有利于硝化细菌。它们会产生足够的MLVSS。一个污泥的年龄tRX>需要4_6天才能实现硝化。健康和充足的硝化细菌的存在是成功硝化的基本要求。第6章讨论了tR和tRX对去除率或去除率的影响。
反硝化作用
10.2.3.1反硝化细菌和化学计量学
反硝化细菌能够通过将废水中的氧化氮转化为逃逸到大气中的N2气体来去除废水中的氧化氮。大多数反硝化生物都是兼性好氧化学有机异养细菌约占活性污泥环境中细菌的80%。下缺氧条件下亚硝酸盐和硝酸盐作为电子受体,而不是O2和有机底物作为电子供体,在极低氧浓度下产生ATP。
反硝化细菌是常见的土壤和水微生物,与粪便废物有关。它们作为生活废水中的粪便生物进入活性污泥过程,并在有游离分子氧的情况下使用。如果使用相同的C源,O2作为电子受体所产生的能量仅比NO_和NO_多7% (McKinney和Conway 1957)。
除异养反硝化外,化学化能自养细菌也可以用H2或还原硫酸盐化合物作为电子受体进行反硝化(Lompe 1992;Beller et al. 2004)。Kuai和Verstraete(1998)显示了限氧自养硝化-反硝化的发生。在低c′和/或缺氧条件下,悬浮污泥或生物膜中的NO_和NO_可以还原为NO、N2O或N2等气体,即使在没有有机碳作为内生反硝化的情况下也是如此(Bernet et al. 2001)。自养反硝化作用是在一些自来水厂用于处理含有NO-/NO-的地下水(Lompe 1992)。我们在这里不讨论这些过程。
主要有五个方面含氮化合物(见式10.38)。硝酸盐是反硝化的初始底物,分子N2是最终产物。如果由于硝酸盐浓度非常高而有机底物浓度相对较低而发生不完全反硝化,则会排放其他中间体,如NO和N2O (Sumer et al. 1996)。
12 3 4
No --* No -* No -* n2o -> n2 (10.38)
NO-的还原是由一个有机体分四步进行的。每一步都可以有条件地被抑制;中间产物可以通过溶解在水中,然后解吸,通过传质进入气泡,然后进入空气而逸出。中间步骤的动力学尚不清楚。到目前为止,还没有确切的氮平衡能够显示有多少no和N2O被生成。通过测量来精确地平衡是非常重要的,但很难做到。
几乎所有的反硝化菌都能利用NO-和NO-。反硝化分解代谢提供了两个生长和能量产生步骤,以甲醇作为能源的简化形式描述(Halling-S0rensen和J0rgensen 1993;劳伦斯和麦卡蒂1969):
^ 6no - + 2co2 + 4h2o (10.39)
^ 3n2 + 3co2 + 3h2o + 6oh - (10.40)
6no + 5ch3oh ^ 3n2 + 5co2 + 7h2o + 6oh - + ag0 (10.41)
然而,这与需氧分解代谢相反,在有氧分解代谢期间不产生羟基离子:
3o2 + 2ch3oh ^ 2co2 + 4h2o (10.42)
有机底物被完全氧化成CO2和H2O.产生的OH-(见公式10.40和10.41)是碱性的;产生的一些二氧化碳被返回到硝化池。该离子根据NH+进水浓度得到部分或全部补偿,并在软水硝化过程中消耗掉。
为了保持活性污泥中足够的碱度,可以向水中加入各种化学物质或碱性物质。这些化学物质包括碳酸氢盐(HCO-)、碳酸盐(COf-)和钙、镁和钠的氢氧化物(OH-)。通常添加以下用于缓冲碱度的化学物质:碳酸氢钠(NaHCO3)、碳酸钙(CaCO3)、碳酸钠(Na2CO3)、氢氧化钙(Ca(OH)2)和氢氧化钠(NaOH)。有时,如果处理硬水,例如柏林(Beelitzhof)的水,其总硬度为15.3°dH,碳酸盐硬度为10.8°dH (BWB 2004),则不需要这样做。
10.2.3.2反硝化化学计量学和动力学
几乎所有的有机物都可以用作底物。对于分解代谢和合成代谢的化学计量学的讨论,甲醇是合适的。与甲醇的一个C原子相关,我们可以这样写(Lawrence and McCarty 1969):
0.926 no - + ch3oh + 0.22 h2co3 ^ o.o5ic5h7o2n + 0.435 n2 + 0.926 hco - + 1.56 h2o
1.49no -+ ch3oh + 0.79h2co3 ^ 0.059c5h702n + 0.72 n2 + 1.49hco -+ 1.84 h2o
根据式(10.13),计算底物利用率和反硝化速率为:
可以得到NO2的相应方程。由式(10.43)可知,真实产量系数YXC/SC和YSC/NO3-N为:
0.051 Mxc 0.051 -12-5 g mol-1 C5H7O2N-C 1.0■12 g mol-1 CH3OH-C
gMLVSS11 gDOC
gXC Msc
0.926 Mno3-n 0.926-14 g mol-1 NO3-N gSC
由式(10.47)和式(10.48)可得式(10.49):
式(10.44)中的NO2分别为:
XC/NO3-N - YXC/SC ' YSC/NO2-N - gNO
0.454
gMLVSS gNO3-N
0.34
gMLVSS gNO3-N
NO3-N o
XC / NO3-N
1假设MLVSS由50%的碳组成。
象征 |
单位 |
硝酸盐还原 |
减少二氧化氮 |
Fmax |
d 1 |
2.6 |
1.5 |
YX /秒 |
g MLVSS (g DOC)-1 |
1 |
1 |
y / n |
g MLVSS (g NOX-N)-1 |
1.2 |
0.8 |
kd |
d 1 |
0.1 |
0.1 |
ks |
mg L-1 DOC |
62.5 |
- |
KNOx-N |
mg L-1 NOX-N |
< 0.14 |
< 0.12 |
因此,反硝化去除1 g NO3-N,产生0.454 g MLVSS;25.5%的CH3OH-C用于合成代谢,74.5%用于分解代谢(见式10.49)。然而,生物质的产量取决于所使用的基质,导致YX/N不同。反硝化细菌可以利用生活废水中常见的大多数有机化合物。几种有机底物如甲醇、醋酸、乙醇、葡萄糖或糖蜜的一部分影响废水如果进行后反硝化(见第10.4.2节),通常会添加到反硝化罐中。
表10.5给出了一些反硝化动力学系数和产率系数。
细菌的特定生长速率既受有机底物浓度的影响,也受NO_或NO_浓度的影响。反硝化动力学可以用双Monod动力学模型和一个附加项来描述,其中包括溶解O2浓度对NO3_ (Batchelor 1982;IAWPRC 1986):
PNO2-N - Pmax,NO2-N
注意,如果使用不同的基材,这三个饱和系数可能会有所不同。
KS + S KNO3 + sNO3
Ks + s kno2 + sno2
10.2.3.3影响反硝化的参数
由式中的动力学观察。(10.51)和(10.52)可以看出,反硝化需要一定的有利条件,如有机底物的存在,c' (c';0),校正pH和T。
充足的有机底物是反硝化的主要控制参数之一。由式(10.48)可知,有机碳与硝酸盐的最佳比例约为YSC/NO3-N = 0.89 g DOC (g NO3-N)_1,此时可能实现完全反硝化。较低比例时,NO3出水浓度增加。当YSC/NO2- n = 0.58 g DOC (g NO2- n)_1时,NO2的值略低。这是通过NO2积累硝化的优点之一(见第10.2.4节)。控制易降解有机物的浓度,可获得较高的反硝化速率。
自由分子氧抑制反硝化,因为氧抑制了硝酸还原酶的形成(Payne 1973)。Wheatland等人(1959)发现c' = 0.2 mg L-1时的反硝化速率约为c' = 0 mg L-1时的一半(KiO = 0.2 mg L-1 O2)。
反硝化作用导致碱度增加。方程中产生的OH-。(10.40)和(10.41)用于生成H2O和生成H+硝化作用。反硝化作用可以在很宽的pH值范围内发生。大多数研究表明,pH 7.0-7.5时反硝化率最高(Halling-S0rensen和J0rgensen 1993年)。
微生物的生长速度和硝酸盐的去除率都受温度的影响。对于低于5°C的废水,由于生物代谢太慢,反硝化受到高度限制。表10.6总结了操作因素有利于反硝化作用。
在+50 mV到-50 mV的氧化还原电位范围内,氧要么不存在,要么只在相对较小的浓度下存在。在+50 mV以上,有氧条件占主导地位。
如果反硝化的碳源可能被耗尽,就会发生内源性反硝化。Adam(2004)观察到在较长时间内(>30 h)反硝化速率恒定反硝化过程没有Bio-P生物。这意味着在这个实验中碳源的种类没有改变和/或耗尽。这是内源性反硝化的典型特征。根据式(10.51),rNO3可以描述为反映内源性呼吸:
内源性反硝化速率通常比使用外部碳源时低。但是,如果细菌浓度在缺氧区的增加,反硝化速率也随之增加(Adam 2004)。内源性反硝化和细菌裂解过程中铵离子浓度升高,细菌浓度降低。
参数 |
最佳范围/值和注释 |
有机碳 |
主要控制参数,比例3:1(有机COD与NO2、NO3) |
是否最优为完全反硝化,且3:2以上会引起增加 |
|
NO2和NO3。 |
|
c ' |
抑制反硝化作用,明显抑制反硝化作用 |
c' > 0.2 mg L-1 O2。 |
|
PH值 |
影响反硝化细菌的酶活性,7.0 < pH |
最佳< 7.5。 |
|
温度 |
反硝化速率随T的增加而增加,直到T=35℃; |
非常低的速率低于5°C。 |
|
氧化还原电位 |
+50 ~ -50 mV, +50 mV以上有氧条件占优势。 |
硝化过程中亚硝酸盐的积累
在一定的工艺条件下,亚硝酸盐的积累促进了铵的氧化速率,超过了亚硝酸盐的氧化速率。找到并优化这些工艺条件是亚硝酸盐积累的关键。以下参数适用于高浓度亚硝酸盐:
•由于亚硝基单胞菌的KNS = 0.3 mg L-1 O2低于硝基细菌的KNB = 1.1 mg L-1 O2,因此溶解氧浓度有限(见表10.3)。
•控制pH以获得一定浓度的HNO2和NH3(见章节10.2.2.2)。
•较高的温度有利于亚硝基单胞菌(T = 28-35°C;见第10.2.5节)。
亚硝基单胞菌和硝酸杆菌的不同K′值(Dombrowski 1991;Wiesmann 1994;Pirsing 1996)表明亚硝酸盐氧化成硝酸盐在低氧浓度下比铵氧化更有限。在高生物量浓度的好氧生物膜反应器中,转化率通常受到氧气从液体转移到生物膜的限制(见第7章)。有限的氧气转移到生物膜导致生物膜表面的溶解氧浓度非常低,因此由于亚硝基单胞菌的K′值较硝酸杆菌低,亚硝酸盐氧化为硝酸盐的限制更有效。为了利用这一特性,大多数关于亚硝酸盐积累的研究都集中在生物膜反应器上(Abeling和Seyfried 1992;加里多等,1997;Bernet et al. 2001;Antileo et al. 2003)。
在某些情况下氨氧化停止在亚硝酸盐阶段,即使c足够高,不限制亚硝酸盐氧化。这可以解释为亚硝酸盐的积累也与氨的抑制有关。Anthonisen等人(1976)发现,在8-124 g m-3 NH3-N浓度时,亚硝基单胞菌的氨抑制作用首先显现出来(见式10.28),而在0.1-1.0 g m-3 NH3-N浓度时,HNO2对硝酸杆菌的选择性抑制作用已经出现。
利用低氧浓度的特点以及亚硝酸单胞菌和硝酸杆菌对氨的不同抑制作用,在悬浮膜生物反应器中观察到74%的亚硝酸盐积累(Choi 2005)。
图10.5为亚硝酸盐积累的硝化反硝化原理图。
与硝酸盐途径(NH+ ^ NO- ^ NO- ^ NO- ^ N2)相比,通过亚硝酸盐途径(NH+ ^ NO- ^ N2)持续积累亚硝酸盐对废水的氮去除有几个好处:
•更快的硝化和反硝化过程的动力学,
•在曝气过程中节省高达25%的能源,
•减少对有机基质的需求,可节省高达40%的成本;
•更高的反硝化率,
•较低的生物量产量(最多为以前的三分之一)。
-
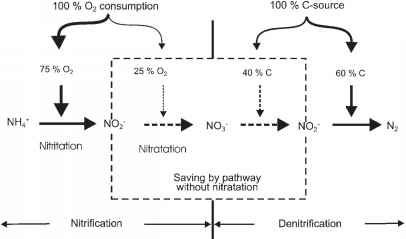
- 图10.5硝化反硝化亚硝酸盐积累示意图。
作为缺点可以提到:
•硝化必须精确地操作和控制,
•自动测量缺氧步骤排出物中的NO2浓度导致运行成本增加。
新型微生物脱氮工艺
的氨氧化厌氧氨氧化是一种新的生物脱氮方法。某些化能自养细菌能够在缺氧条件下以亚硝酸盐作为电子受体,将电子供体铵氧化为氮气(Mulder 1992;穆德等,1995;Jetten等人,1998;Helmer et al. 2001):
NH+ + NO- ^ N2 + 2H2O + AG0其中:AG0 = -359 kJ…-380 kJ (mol NH+)-1
该细菌属于普朗克菌属的稀有目,其中最重要的成员是普朗克菌属和倍氏菌属。目前属为Brocadia和Kuenenia(淡水种)和Scalindua(海洋种)。催化厌氧氨氧化反应的细菌是自养的,这意味着亚硝酸盐转化为N2的过程不需要使用有机碳。该工艺的特点是污泥产量低,曝气能量大幅减少60%和化学中和。二氧化碳净排放量大幅减少。与常规脱氮相比,该方法的成本降低幅度相当大(Van Dongen et al. 2001)。
SHARON工艺(单反应器系统对亚硝酸盐进行高活性氨去除的缩写)旨在促进高浓度废水中亚硝酸盐的生物脱氮(Van Dongen et al. 2001),它具有几个优点(见第10.2.2节)。它的pH值控制非常重要。亚硝酸盐氧化在pH值较低的区域(HNO2浓度较高)可以被抑制,而在氧浓度较低的区域则受到限制(Van Kempen et al. 2001)。该过程在高温(>25°C)下运行,有选择性地促进快速生长的氧化铵剂,而硝化杆菌可以从系统中被冲洗出去。其特点是完全没有污泥滞留(tRX = tR),因为污泥的生长和冲刷处于平衡状态(Hellinga等人,1998年;Van Kempen et al. 2001)。
基于这种自养脱氮概念的过程已在a中被详细描述和研究序批式反应器SBR (shy et al. 1998;Fux等人,2002),在连续流动移动床试验装置(Helmer等人,2001),在a流态化床反应器(Van de Graaf et al. 1996)和悬浮SHARON_ANAMMOX系统(Hellinga et al. 1998;Van Dongen et al. 2001)。该联合除氮新方法可技术应用于高铵无DOC工业废水。
经典的自养硝化/异养反硝化方法和部分硝化/自养厌氧氨氧化(ANAMMOX)厌氧的成本估算污泥消化证明部分硝化/厌氧氨氧化比传统的硝化/反硝化更经济(Fux和Siegrist 2004)。基于STOWA(1996)对污水处理能力为50万inh的废水进行了不同脱氮技术的全面成本估算。
10.3
强化生物除磷
活性污泥系统的强化生物除磷首次报道于20世纪60年代末(Vacker et al. 1967)。不动杆菌(Acinetobacter sp.),特别是沃菲氏乳杆菌(L. woffii)被确定为负责在其细胞中积累过量磷酸盐的生物,如果它们有短链挥发性脂肪酸(VFAs)可用,特别是醋酸,作为饲料(Fuhs和Chen 1975)。
生物除磷是通过创造有利于聚磷生物(PAOs)生长的条件来实现的。一个初始厌氧区允许PAOs吸收VFAs进入细胞,并以聚羟基丁酸酯(PHF)的形式储存。在此之前储存的聚磷酸盐被氧化并用作能源,产生ATP;并因此被释放到液相中(图10.6)。有机物的厌氧吸收与聚磷酸盐的积累有内在的关系。
坑
坑
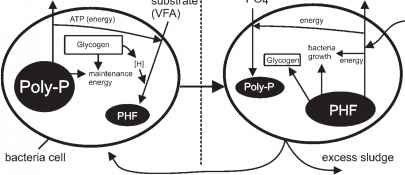
厌氧好氧
图10.6强化生物除磷机理;所示为每次过程的开始(Wentzel et al. 1991)。
厌氧好氧
图10.6强化生物除磷机理;所示为每次过程的开始(Wentzel et al. 1991)。
在混合液到达好氧区后,储存的PHF被PAOs用于细胞生长,并为从所有可用的正磷酸盐转化聚磷酸盐提供能量,也用于合成聚葡萄糖(糖原)。经过厌氧和好氧条件,PAOs充分建立,并在几周后成为生物量群落的主导。PAO是唯一一种能够在第一个厌氧反应器中存储底物并在第二个反应器中氧化它们的细菌好氧反应器.这只能通过Poly-P存储的富集来实现。这种含有高浓度聚磷酸盐的PAOs的富集导致了生物除磷的建立。该过程的净消除是由于细菌细胞的生长和当磷酸盐被吸收到高于厌氧阶段释放的水平时剩余污泥的去除(见下图10.7)。
除磷动力学模型
为了获得动力学和化学计量学信息,我们需要做如下假设:
•反应堆作为cstr运行(见章节6.2.2),
•过程处于稳态,
•使用醋酸酯作为基材。
有机底物代谢的生化途径与聚磷酸盐的储存密切相关。有机底物与聚磷酸盐之间有明显的关系。厌氧阶段底物的吸收和磷的释放可以用醋酸盐和PO4-P的平衡来描述
246年10生物养分去除混合点M
-
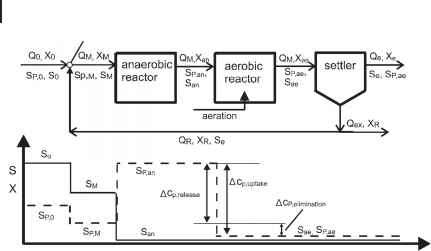
- 图10.7 CSTR两段生物除磷(AO工艺,Phoredox),磷和底物浓度分布图。
通过在好氧反应器前安装一个厌氧反应器,将流程图与图6.3进行了扩展。
10.3.2.2厌氧区
以下平衡是有效的厌氧CSTR容量Van:
0 = QM(SM-San) - rs,anVan (10.54)
PO4-P:
0 = QM(SP,M-SP,an) + ^ Van (10.55)
生物量X:
:
YSC/PO4-P = S M Sa" = S M Sa" (10.57)
SP,一个SP,M SP,一个SP,M
和:
黄嘌呤Xm
SM -San, SM为与回流污泥混合后的醋酸盐浓度,San为厌氧反应器中醋酸盐浓度,SPan为厌氧反应器中PO4-P浓度,SP,M为与回流污泥混合后的PO4-P浓度,rSan为乙酸盐摄取速率,SPPan为厌氧反应器中细菌细胞中聚磷的浓度,SPPM为细菌细胞与回流污泥混合后的聚磷浓度。
在已知反应器体积Van和流速Qm的情况下,为了确定SP,首先需要知道厌氧阶段底物转化率rSAn与乙酸盐和正磷酸盐浓度的关系。用速率系数k代替比最大生长速率pmax和产量系数YXC/SC。修正的双monod动力学可以通过实验验证(Wentzel et al. 1987;高1995;罗曼斯基1999):
YXC/SC KS+ Sa
如果nPP = 0,则不能占用任何衬底物。对于nPPP KPP,乙酸吸收速率rS仅为San和Xan的函数;而对于Sanp KS,它只取决于Xan。
10.3.2.3好氧区
以下平衡值适用于好氧CSTR体积Vae:
0 = Qm (San Sae) - rS aeVae (10.61)
0 = QM(SP,an-SP,ae) - Y/S,ae Vae (10.62)
生物量X:
0 = Qm (Xan Xae) + Vae (10.63)
:
一个,一个
SP,ae SP,an SPP,ae-SPP,an和:
在好氧区,磷的吸收和底物转化率受到液相正磷酸盐和细菌细胞中以PHB形式储存的碳源的影响。它们彼此之间的连接非常紧密,我们假设细菌的生长是基于细胞内PHB发生的:
YSC/PO4-P = ^ J" = S an Sae (10.64)
Pmax SP,Ae nPHB c " ^ ^
rPae = -o——Xae-:——;——(10.66)
YXC/PO4-P KPAe + SPAe KPHB + nPHB K +c
r = Pmax x SP ae nPHB c (10 67)
YXC/PHB KP,ae + SPae KPHB+nPHB K +c
:
注意,底物现在以PHB的形式存储在细胞内。
几位作者开发了各种生物除磷模型(Wentzel et al. 1986;Tsuno等,1987;Ante和Vofi 1995;高1995;Henze等,1995;罗曼斯基1999)。但目前还没有描述生物除磷动力学的标准模型。它的速率主要取决于厌氧反应器和好氧反应器中聚磷积累细菌的浓度以及方程中的浓度。(10.59),(10.66)和(10.67)。这些方程还没有得到充分的验证,需要进一步的研究。
批量实验结果
图10.8显示了分批实验中S和SP的浓度分布,显示了磷的净消除(Romanski 1999)。
在厌氧期,义务性好氧聚磷菌(PAOs)吸收底物(如醋酸盐)并将其作为脂质储备物质(PHB)储存。同时,
-
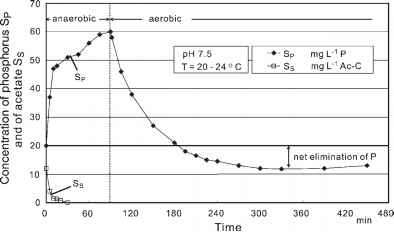
- 图10.8分批实验中SS和SP的浓度分布(Romanski 1999)。
ly,细胞内的聚磷酸盐被部分利用为能量来源并被释放,导致SP从20 mg l1 PO4-P增加到60 mg l1 PO4-P,这与PHB的合成密切相关。只要醋酸盐存在,聚磷酸盐就以很高的速率被释放。随后,通过细菌裂解形成的其他底物部分转化为低脂肪酸,导致p释放较慢。
在接下来的好氧阶段,正磷酸盐被吸收到细菌细胞中,而PHB被用于生长。正磷酸盐的浓度SP从厌氧间歇试验开始时的初始浓度20 mg L_1下降到12 mg L_1 PO4-P。8 mg L_1 PO4-P的差值是磷的净去除率。更多的磷酸盐被好氧吸收比厌氧释放,因为它是丰富的生物量,由于细菌的生长,被去除多余的污泥。
影响生物除磷的参数
充足的VFAs供应是成功的生物除磷的关键因素之一,因为它与聚磷酸盐的释放或磷酸盐的吸收有很强的关系。VFAs要么是进水中易生物降解底物的一部分,要么是在厌氧区通过兼性发酵形成的需氧细菌.相比之下,产甲烷菌不能在从无氧到有氧条件变化的系统中生长。
如果有足够的溶解氧存在,PAOs可以在好氧区以适当的速度生长。但应尽量减少将O2或NO2和NO3引入厌氧区,因为它优先用作末端电子受体,这减少了PAOs可摄取的VFAs的数量(Hascoet和Florentz 1985)。结果,好氧区对磷酸盐的吸收减少。
的固体保留时间tRX必须足够让PAOs生长,并能显著影响磷去除率。增加厌氧tRX将增加有机物的发酵,从而增加VFAs的产量和总去除率。一个低水力停留时间tR有利于优化工艺。影响生物除磷性能的主要参数如表10.7所示。
降低厌氧区温度可降低发酵速率。PAOs受pH值降低的影响比硝化细菌小(美国环保局1993年)。整体磷酸盐去除可能随着pH值的降低而下降,因为在较高的H+浓度下,吸收乙酸盐需要更多的能量,因为未解离的乙酸盐浓度降低了。
细菌nPP的磷含量可能对磷去除率有显著影响,因为它与PAOs释放和吸收磷的能力密切相关。典型的平均nPP值为细菌质量的5_7%,在某些情况下可获得高达12_15%的值,这取决于工艺配置。常规活性污泥的nPP通常在1.5%至2.0%之间(Grady et al. 1999)。
表10.7影响BPR过程的参数。
参数
最佳范围/值和注释
足够的VFAs浓度是有益的。低的浓度
VFAsa)的浓度降低了厌氧区磷的释放,导致好氧区磷摄取相应降低。
建议生长PAOs的tRX = 1.0-1.5 d。
c' c'限制VFAs的形成,因为VFAs是在严格的厌氧条件下正确形成的。
低温可以减少VFAs的形成和PAOs的活性。
PAOs对pH变化的敏感性低于硝化细菌。
降低pH值对磷去除率有不利影响。
厌氧区NO3的存在减少了磷的释放,从而导致磷的减少
好氧区磷的摄取。
MLSS中P的含量与PAOs释放和吸收P的能力密切相关。
a)挥发性脂肪酸。
10.4
生物养分去除过程
序言
生物养分去除工艺是活性污泥工艺的改进,将缺氧和/或厌氧区与有氧区提供氮和/或磷去除。可以进行多种配置,从而产生各种性能能力和操作特性,如表10.8所示。
本节描述和讨论提供氮或磷或两种成分去除的生物去除系统。
脱氮工艺
生物脱氮的主要过程包括好氧硝化阶段和缺氧反硝化阶段。图10.9a显示了一种两阶段生物脱氮系统(Ludzack and Ettinger 1962),称为改进的Ludzack -Ettinger (程序流程.他们首次提出了在进水废水中使用可生物降解有机物的单一污泥硝化-反硝化工艺。
表10.8生物养分去除过程中不同区域的特征。
区 |
生物化学转换 |
函数 |
删除组件 |
厌氧 |
磷释放 |
PAOsa的富集) |
磷 |
易形成 |
碳 |
||
生物可降解有机物 |
|||
通过发酵 |
|||
挥发性物质的吸收和储存 |
|||
由PAOs生成脂肪酸 |
|||
缺氧 |
反硝化作用 |
将NO3-N还原为N2 |
氮 |
外源性代谢 |
反硝化的选择 |
碳 |
|
兼性底物 |
细菌 |
||
异养生物 |
|||
碱度的产生 |
PO4b的吸收) |
磷 |
|
有氧 |
硝化作用 |
NH4-N氧化为NO2-N |
氮 |
和/或NO3-N |
|||
碱度消耗 |
气体脱氮 |
||
剥离 |
|||
磷的吸收 |
聚磷酸盐的形成 |
磷 |
|
贮存和贮存的代谢 |
PO4c的吸收) |
||
外生底物的PAOs |
|||
外源性代谢 |
碳 |
||
基质被异养 |
a)聚磷生物。
b)在易于生物降解的有机物存在时,几乎所有的PO4-P都被吸收了。
c)如果在缺氧阶段使用了所有易生物降解的有机物,没有完全吸收PO4-P,则在好氧阶段使用有机裂解产物去除额外的PO4-P。
a)聚磷生物。
b)在易于生物降解的有机物存在时,几乎所有的PO4-P都被吸收了。
c)如果在缺氧阶段使用了所有易生物降解的有机物,没有完全吸收PO4-P,则在好氧阶段使用有机裂解产物去除额外的PO4-P。
-
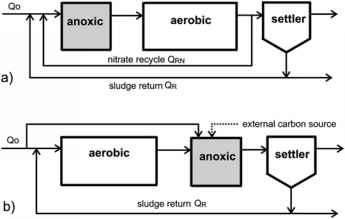
- 图10.9 (a)反硝化前(b)反硝化后生物脱氮过程。
反硝化的缺氧阶段位于生成NO的好氧阶段的前面。循环流QRN和QR都有目标硝酸盐排出量,这抑制了可能的反硝化量。实际出水氮浓度由工艺总氮进水浓度和总循环流量QRt与进水流量Q0的关系nRN决定。
它的优点是消耗了废水中所含的有机物,而不添加额外的有机底物。该工艺的一个缺点是剩余的NO-在形成后被排出,因为典型的最大循环流量为QRN;5(Q0 + QR)。在较高QRN时,泵送能耗过高,导致运行成本高,但脱氮量没有明显增加。该过程具有良好的硝化作用和良好的反硝化程度,直至SN;4-8 mg L-1 Nt。为了将去除效率提高到SN < 3.0 mg L-1 Nt的出水水平,进一步发展了MLE工艺,产生了四级Bardenpho过程巴达德(1973)。它涉及到一个二级缺氧和一个小型好氧反应器的过程扩展。
与MLE过程相反(图10.9a),好氧区位于缺氧区前面(图10.9b)。为了利用废水中的可生物降解有机物,一部分进水绕过第一阶段,进入缺氧阶段。只有污泥被返回到初始需氧过程.降低了泵送QRN的能耗。如果在某些情况下,进水或好氧硝化阶段的出水中不存在足够的有机物,则在缺氧阶段添加补充的无n碳源,如甲醇或醋酸盐。如果添加的补充底物价格低且需要非常低的NH4浓度,则此配置可能有用。这种配置可以通过一个较小的好氧区扩展到缺氧阶段以外,以从缺氧阶段去除剩余的碳和NH4(在废水旁路的情况下)。添加无氮碳源可以提高工艺效率,但会增加化学成本。
化学和生物除磷
在讨论生物除磷过程之前,我们将简要说明化学沉淀法除磷。生活废水中磷的主要成分是正磷酸盐PO4-P(图10.1)。用Al3+和Fe3+盐沉淀可从废水中分离。通常会同时使用两个不同的过程降水发生在一个有氧箱里活性污泥厂在那里,Fe3+是由较便宜的Fe2+快速氧化而产生的。如果应用FeSO4,我们写:
PO4- + FeSO4 ^ FePO4 I + SO2- + e- (10.69)
不溶性FePO4主要在活性污泥颗粒内形成絮凝体,可作为剩余污泥分离。
在一些北方国家,首选在二级澄清器之雷竞技手机版app后进行沉淀,使用反应器进行沉淀,使用沉降器进行絮凝物分离。反应堆没有充气。因此,使用Al3+和Fe3+盐代替Fe2+盐。如果使用Fe2(SO4)3,我们写:
2PO3- + Fe2(SO4)3 ^ 2FePO4 I + 3SOJ- (10.70)
以获得较大的絮凝体沉降速度,聚合物作为絮凝剂加入。
如表10.1所示,溶解的无机聚磷酸盐和有机磷以及颗粒磷是城市废水的组成部分。它们只能通过吸附和共沉淀法部分分离。
厌氧过程又称好氧(或好氧)过程,又称AO过程Phoredox)是一种生物除磷方法(见图10.7)。在前面放置一个厌氧反应器常规活性污泥法导致使用进水有机质厌氧形成PHB。通过最小化硝化作用和最大限度地增加聚磷储存细菌的产量,可以获得高磷去除率。如果计划在农业中使用,高固体生产是有益的,因为高磷含量生物质的生产是最大化的。厌氧区包含在主要工艺流中,因此被视为主流的生物除磷工艺。
脱氮除磷工艺10.4.4.1不同性能水平
许多配置已经发展为生物脱氮除磷的联合过程,包括厌氧、缺氧和好氧区。由于硝酸盐对除磷的负面影响,应尽量减少和控制硝酸盐再循环到厌氧区;这是选择和设计这些工艺的关键考虑因素。
AAO工艺(图10.10a)是厌氧和好氧MLE工艺(图10.9a)脱氮和厌氧和好氧Phoredox工艺(图10.7)脱磷的组合。内部循环流量通常为Qrn = (2-4)-(Q0 + Qr)。的氮去除率与MLE法的除磷效果相似,但有时比AO法的除磷效果略低。
部分硝酸盐随着回流污泥进入厌氧区,QRN过低会对除磷产生不利影响。进水中有机物含量对除磷影响最大。如果有机物含量足够高,可以同时去除磷和氮,则硝酸盐循环对出水水质影响不大,但如果有机物含量较低,则对去除率影响较大。将硝酸盐转化为N2的反硝化也可以部分在沉降器中的污泥毯中进行,这减少了硝酸盐循环到厌氧区,并导致细菌絮凝体被冲洗出系统。设计不当
-
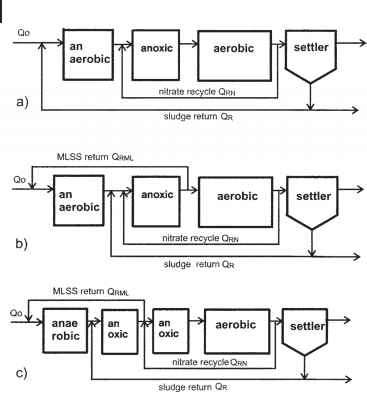
- 图10.10同时去除氮和磷的工艺:(a) AAO工艺;(b)污泥只返回到缺氧阶段,部分无O2和无alo3活性污泥从缺氧阶段返回到厌氧阶段;(c)两个缺氧阶段。
污泥毯会导致污泥膨胀、结块和漂浮,降低系统效率。
为了消除硝酸盐循环对磷去除率的负面影响,为了避免向厌氧阶段输入一些氧气,开发了一种只将污泥返回到缺氧阶段的工艺(图10.10b)。在缺氧阶段后,部分流动不含no3,不含no3浓缩污泥循环进入厌氧阶段。
除此之外,缺氧区可分为两个(最多四个)反应器(图10.10c)。第一个缺氧反应器接收回流污泥流并反硝化,第二个反应器接收硝酸盐再循环流并反硝化。反硝化混合液从第一厌氧反应器的出水再循环到厌氧区,为进水废水提供细菌。其优点是防止了二次缺氧对污泥回流的影响。
许多其他的生物去除氮和磷的营养过程已经开发出来(Randall等人,1992年;Grady et al. 1999)。所采用的工艺和装置设计取决于处理目标、法规、待处理废水的成分和运行成本
继续阅读:信息Kgl
这篇文章有用吗?






